Температура - диссоциация - карбонат
Cтраница 2
Для серии экспериментов была отобрана накипь из кипятильной трубы котла низкого давления ( 10 - 15) - 10s Па, питавшегося неочищенной речной водой. Первый эндотермический эффект ( 400 С) на термограмме соответствует температуре дегидратации гидроксида магния, второй ( 520 С) - температуре дегидратации гидроксида кальция и третий ( 880 С) близок к температуре диссоциации карбоната кальция, которая для чистого продукта равна 900 С. Таким образом, эта накипь состоит в основном из карбоксидов магния и кальция и из карбоната кальция. [16]
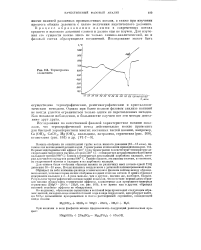 |
Термограмма ксопотлита. [17] |
Накипь отобрана из кипятильной трубы котла низкого давления ( 10 - 15 атм), питавшегося неочищенной речной водой. Первый эндотермический эффект ( 400 С) на термограмме соответствует температуре дегидратации гидроокиси магния, второй ( 520 С) - температуре дегидратации гидроокиси кальция и третий ( 880 С) близок к температуре диссоциации карбоната кальция, которая для чистого продукта равна 900а С. Таким образом, эта накипь состоит, в основном, из гидроокисей магния и кальция и из карбоната кальция. [18]
Количество выделившейся двуокиси углерода или точнее давление двуокиси углерода в такой закрытой гетерогенной системе зависит лишь от температуры, как было указано на стр. Если двуокись углерода удаляется из системы, то, естественно, карбонат будет разлагаться полностью, как, например, в печи для обжига извести. Температура диссоциации карбоната изменяется в зависимости от природы катиона. [19]
При организации технологического процесса очистки дымовых газов от сернистого ангидрида в реальных условиях получение необходимых окислов металлов, очевидно, должно быть основано на использовании природного сырья в виде минералов: известняка, мела, магнезита, доломита, сидерита и других. В связи с этим представляет практический интерес выяснение термодинамических характеристик реакции взаимодействия сернистого ангидрида с карбонатами рассматриваемых металлов в присутствии кислорода. В табл. 36 представлены подсчеты значений изобарных потенциалов этих реакций при разных температурах. Из табл. следует, что термодинамически возможно осуществлять очистку газов от сернистого ангидрида в присутствии кислорода с помощью карбонатов кальция, магния, железа, цинка и марганца в широком интервале от 300 до 1000 С. Указанный интервал охватывает температуры, превышающие температуру диссоциации рассматриваемых карбонатов. Следовательно, фактически выше этих температур диссоциации справедливы закономерности, относящиеся к реакциям взаимодействия с сернистым ангидридом уже окислов этих металлов, а не их карбонатов. В условиях температур ниже температур диссоциации карбонатов направление реакций в сторону образования сульфатов металлов вместо их карбонатов определяет эффект совместного присутствия сернистого ангидрида и солей слабых кислот. [20]
При организации технологического процесса очистки дымовых газов от сернистого ангидрида в реальных условиях получение необходимых окислов металлов, очевидно, должно быть основано на использовании природного сырья в виде минералов: известняка, мела, магнезита, доломита, сидерита и других. В связи с этим представляет практический интерес выяснение термодинамических характеристик реакции взаимодействия сернистого ангидрида с карбонатами рассматриваемых металлов в присутствии кислорода. В табл. 36 представлены подсчеты значений изобарных потенциалов этих реакций при разных температурах. Из табл. следует, что термодинамически возможно осуществлять очистку газов от сернистого ангидрида в присутствии кислорода с помощью карбонатов кальция, магния, железа, цинка и марганца в широком интервале от 300 до 1000 С. Указанный интервал охватывает температуры, превышающие температуру диссоциации рассматриваемых карбонатов. Следовательно, фактически выше этих температур диссоциации справедливы закономерности, относящиеся к реакциям взаимодействия с сернистым ангидридом уже окислов этих металлов, а не их карбонатов. В условиях температур ниже температур диссоциации карбонатов направление реакций в сторону образования сульфатов металлов вместо их карбонатов определяет эффект совместного присутствия сернистого ангидрида и солей слабых кислот. [21]
Страницы: 1 2