Температура - культивирование
Cтраница 1
Температура культивирования; пленки нет; пленка есть - сплошная, тонкая, иризирующая, толстая, слизистая, сухая, гладкая, складчатая. [1]
Снижение температуры культивирования ведет к повышению степени ненасыщенности клеточных липидов. [2]
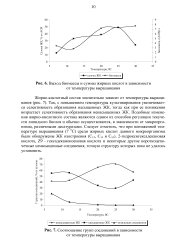 |
Соотношение групп соединений в зависимости от температуры выращивания. [3] |
Так, с повышением температуры культивирования увеличивается селективность образования насыщенных ЖК, тогда как при ее понижении возрастает селективность образования ненасыщенных ЖК. Подобные изменения жирно-кислотного состава являются одним из способов регуляции текучести липидного бислоя и обычно осуществляются, в зависимости от микроорганизма, различными десатуразами. Следует отметить, что при пониженной температуре выращивания ( 7 С) среди жирных кислот данного микроорганизма были обнаружены ЖК изостроения ( Си, Си и Cie), 2-гидроксигексадекановая кислота, Z9 - гексадекамоноеновая кислота и некоторые другие короткоцепо-чечные ненасыщенные соединения, точную структуру которых пока не удалось установить. [4]
Известно большое взаимное влияние температуры культивирования и рН среды: если понижение температуры культивирования ведет к увеличению общей ненасыщенности синтезируемых липидов, то снижение рН среды повышает их насыщенность. Оказывая определенное воздействие на ферменты синтеза липидов, оба эти фактора позволяют в известной степени управлять биосинтетическими процессами в микробной клетке. [5]
На процессы биосинтеза липидов у микроорганизмов оказывают влияние также рН среды и температура культивирования. Так, повышение рН среды увеличивает содержание в составе дрожжевых липидов свободных жирных кислот, фосфолипидов и уменьшает содержание триацилглицеринов. При снижении рН увеличивается общая ненасыщенность липидов. [6]
Известно большое взаимное влияние температуры культивирования и рН среды: если понижение температуры культивирования ведет к увеличению общей ненасыщенности синтезируемых липидов, то снижение рН среды повышает их насыщенность. Оказывая определенное воздействие на ферменты синтеза липидов, оба эти фактора позволяют в известной степени управлять биосинтетическими процессами в микробной клетке. [7]
Специфичным является воздействие на дрожжи, выделяющие липиды, таких факторов, как температура культивирования и рН среды. Снижение температуры способствует тому, что дрожжи постепенно теряют способность к экскреции липидов, но зато начинают выделять значительные количества внеклеточных полисахаридов. Аналогично действует и снижение активной кислотности среды. Подобное явление свидетельствует о большой взаимосвязи процессов биосинтеза внеклеточных липидов и полисахаридов, которые образуются из одних и тех же предшественников. [8]
Так, максимальное поглощение метана культурой Methanomonas carbonatophila наблюдается при сравнительно низком значении начального рН ( около 6 5) и температуре культивирования 30 - 36 С. Для роста Methanomonas methanooxidans оптимальными параметрами процесса роста являются рН 6 1, температура 30 С. Pseudomonas methanica при выращивании на среде с нитратом натрия лучше растет в интервале рН от 6 6 до 8 0, на среде с сернокислым аммонием оптимум рН сдвигается в кислую зону. [9]
Понижение или повышение температуры приводит к снижению содержания фосфоглицеридной фракции с одновременным увеличением содержания фракции триацилглицеринов. Общее содержание липидов мало зависит от температуры культивирования. Считается, что изменение температуры выращивания оказывает влияние главным образом на скорость роста и накопление биомассы, в меньшей степени влияя на процентное соотношение липидов в клетке. Как следствие снижения выхода биомассы наблюдается снижение общего выхода липидов на единицу используемых редуцирующих веществ. [10]
 |
Липиды архебактерий. [11] |
При повышении температуры количество цепей, содержащих циклические группировки, возрастает, ациклических - снижается. Кроме того, в зависимости от температуры культивирования меняется число колец в цепи. [12]
В такой заполненный сосудик герметически вводят электрохимический датчик растворенного кислорода и при постоянном перемешивании пробы культуры через определенные интервалы времени ( или непрерывно, в зависимости от конструктивных особенностей используемой схемы) проводят измерение концентрации растворенного кислорода. При более строгой постановке эксперимента изъятую пробу культуры помещают в несколько сосудиков, снабженных перемешивающим устройством и находящихся при температуре культивирования. [13]
Лаг-фаза не наблюдается, если молодые клетки быстро переносятся из аппарата в аппарат в совершенно идентичные условия окружающей среды ( рН, температура, концентрация и состав питательных веществ, окислительно-восстановительный потенциал и пр. Ее также не бывает, если производится большой засев ( 20 - 30 млн. бактерий на 1 мл среды) или если при посеве клеток увеличивается температура культивирования. При любом отклонении от первоначальных условий культивирования, достигающих пороговых значений, появляется лагфаза той или иной продолжительности. [14]
Известно, что насыщенные жирные кислоты, входящие в состав липидов, имеют более высокую точку плавления по сравнению с ненасыщенными. Уже давно было замечено, что липиды термофилов имеют более высокие температуры плавления, чем липиды мезофилов, что достигается возрастанием содержания насыщенных жирных кислот в мембранах при повышении температуры культивирования. На основании этих данных и было высказано предположение, что липиды играют определенную роль в молекулярных механизмах термофилии, способствуя термостабильности мембран, и что нижняя температурная граница роста термофилов определяется температурой плавления мембранных липидов. [15]
Страницы: 1 2