Температура - начало - восстановление
Cтраница 2
С повышением давления температура начала восстановления катализатора под действием рабочей смеси понижается. Для давления 1 1 МПа она составляет 600 С, а для 2 1 МПа - 500 С. [16]
Отмечается связь между температурами начала восстановления марганца шлака углеродом, плавления и перехода примесной проводимости в собственную. [17]
Гравиметрическим методом [12] определены температуры начала восстановления трихлоридов, равные, соответственно, для самария - 525 С, европия - 275 С и иттербия - 460 С. Изучено влияние температуры и парциального давления водорода на скорость восстановления трихлоридов. [18]
Эти группы руд различаются уже по температурам начала восстановления газами. Сырой бурый железняк начинает восстанавливаться с заметными скоростями при 220 С, в то время как сырой магнитный железняк лишь при 400 С. Скорость последующего восстановления бурого железняка значительно превышает скорость восстановления магнитного железняка. Это связано не только с физическим состоянием руды ( магнитный железняк плотен, а бурый железняк порист), но и с составом, кристаллической структурой и аллотропическим состоянием окислов железа, так как различия сохраняются и при измельчении руд. Как правило, разновидности окислов железа, полученные при пониженных температурах, обнаруживают большие скорости восстановления. Естественный сырой магнитный железняк, содержащий магнитную окись железа, образованную в изверженных породах при высоких температурах, дает малые скорости восстановления. В то же время магнитная окись железа, образующаяся в процессе восстановления бурых железняков из Fe2O3, восстанавливается со значительно большими скоростями, чем Fe3O4 магнитного железняка. [19]
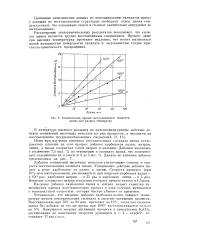 |
Кинетические кривые восстановления силиката цинка для разных температур. [20] |
Установлено, что введение добавки карбоната калия снижает температуру начала восстановления силиката и энергию активации процесса, Восстановление при 700 за 90 мин. Кажущаяся энергия активации процесса в присутствии КаСОз, рассчитанная по константам скорости уравнения а 1 - exp ( At), составляет 17 ккал. [21]
Для МоО3, СиО и № 2О3 были найдены следующие температуры начала восстановления: 475, 460 и 500 С. [22]
Аналогичного эксперимента не удалось сделать в условиях синтеза днметилдихлорсилана, поскольку температуры начала восстановления однохлористой меди кремнием и образования диметилди-хлорсилана близки, вследствие чего трудно различить оба процесса. [23]
Температура, которой соответствует равенство давлений кислорода в обеих стадиях, является температурой начала восстановления окисла углеродом. С термодинамической точки зрения, разделение процесса восстановления на две стадии вполне оправдано, несмотря на то, что истинный механизм взаимодействия может быть иным. [24]
Однако при получении силикоалюминия восстановленный алюминий переходит в раствор с кремнием и железом, в результате равновесие реакции сдвигается вправо и температура начала восстановления понижается. Применение силикоалюминия для раскисления экономически более выгодно, чем применение чистого алюминия, так как расход электроэнергии на тонну чистого алюминия существенно ( на 40 - 50 %) выше, чем на тонну алюминия в силикоалюминии. [25]
Точки пересечения кривых 2 - 12 изменения свободной энергии образования окислов металлов с кривой / изменения свободной энергии образования СО характеризуют температуру начала восстановления окислов металлов углеродом. Выше точек пересечения металлы по их сродству к кислороду меняются местами, и реакции восстановления будут протекать в обратном направлении. Это обстоятельство может привести при высоких температурах не только к восстановлению окислов металлов углеродом, но и к вытеснению, например, алюминием и кремнием тех металлов, окислы которых при данных температурах имеют большие величины энергии образования. [26]
Рассмотрим применение термографии к изучению некоторых процессов, протекающих при формировании, работе и регенерации катализаторов: превращение аморфного состояния в кристаллическое; определение фазового состава катализаторов; определение температуры начала восстановления окисных катализаторов; влияние добавок на вид получаемых термограмм; применение термографии к изучению процессов регенерации катализаторов; термозесовой метод анализа катализаторов; определение температуры зажигания некоторых катализаторов. [27]
Рассмотрим применение термография к изучению некоторых про -, цессов, протекающих при формирований, работе и регенерации катализаторов: превращение аморфного состояния в кристаллическое; определение фазового состава катализаторов; определение температуры начала восстановления окисных катализаторов; влияние добавок на вид получаемых термограмм; применение термографии к изучению процессов регенерации катализаторов; термовесовой метод анализа катализаторов; определенив температуры зажигания некоторых катализаторов. [28]
В табл. 60 приведены температурные условия восстановления окислов до металлов и карбидов. За температуру начала восстановления берется та температура, при которой давление СО достигает 1 атм. Из данных этой таблицы видно, что при восстановлении двуокиси кремния до карбида кремния требуется значительно меньшая температура, чем при восстановлении до кремния. [29]
Железо также восстанавливается углеродом и растворяется в карбиде хрома. Это облегчает условия восстановления хрома и температура начала восстановления хрома понижается. Однако при этих температурах скорость восстановления хрома очень мала. Чтобы получить приемлемые для практики скорости восстановления, а также достаточно жидкоподвижный шлак, процесс ведут так, чтобы температура металла была 1650 С, а шлака 1750 - 1800 С. Все это приводит к тому, что при использовании углерода в качестве восстановителя феррохром получается с высоким содержанием углерода. Степень восстановления кремния зависит главным образом от температуры и активности кремнезема в шлаке. В феррохром переходит также часть фосфора и серы, вносимых с шихтой. Готовый углеродистый феррохром разливают в плоские изложницы. При этом слиток получается толщиной до 200 мм, что облегчает разделку сплава. [30]
Страницы: 1 2 3