Температура - плавление - кислота
Cтраница 2
Этим можно, по-видимому, объяснить такое большое расхождение в значениях температуры плавления кислоты, когда не только скорость нагревания образца, но и способ его загрузки ( с предварительным плавлением или без него) существенно влияют на результаты определения. [16]
При плавлении фталевая кислота частично превращается в ангидрид, что является причиной нерезкой температуры плавления кислоты. [17]
У кислот нормального строения наблюдается интересная закономерность: при общем повышении температуры кипения с увеличением числа углеродных атомов температуры плавления кислот с четным числом углеродных атомов выше, чем температуры плавления соседних кислот с нечетным числом углеродных атомов. [18]
На поверхности активных металлов смазочное действие жирной кислоты продолжается до более высоких температур, на 50 - 70 выше температуры плавления кислоты и близкой к температуре плавления соответствующего мыла жирной кислоты. При применении для смазки раствора мыла данной жирной кислоты и данного металла наблюдается такая же предельная температура эффективности, как п для раствора жирной кислоты на активном металле. Это доказывает, что жирные кислоты в условиях смазки реагируют с поверхностью активных металлов. [19]
У кислот нормального строения наблюдается интересная закономерность: температуры плавления кислот с четным числом углеродных атомов выше, чем температуры плавления соседних кислот с нечетным числом углеродных атомов. Это явление объясняют различным пространственным расположением метильной и карбоксильной групп относительно друг друга. [20]
Колбу необходимо установить от поверхности плиты на расстоянии 8 - 10 см. в противном случае реакция начинается сразу, протекает бурно и температура плавления кислоты снижается. [21]
Анализ серебряной соли янтарной кислоты и титрование ее и щавелевой кислоты раствором едкого кали подтвердили предположение, которое было сделано на основании температуры плавления кислот. [22]
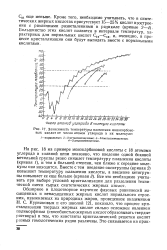 |
Зависимость температуры плавления монокарбоно-вых кислот от числа атомов углерода в их молекуле. [23] |
На рис. 18 на примере монокарбоновой кислоты с 18 атомами углерода в главной цепи показано, что введение одной боковой метильнои группы резко снижает температуру плавления кислоты ( кривая 1), и тем в большей степени, чем ближе к середине молекулы она находится. Все это необходимо учитывать при выборе условий кристаллизации для разделения технической смеси сырых синтетических жирных кислот. [24]
Найденным при помощи рентгеноструктурного анализа зигзагообразным характером длинных цепей может быть объяснена хорошо известная периодичность свойств четных и нечетных членов гомологического ряда ( см., например, температуры плавления кислот, стр. Периодичность внутри ряда естественно объясняется монотонным возрастанием длины цепи при полном сохранении характера взаимного расположения цепей. Это различие лежит в симметрии молекулы. [25]
Одна из кристаллических кислот имеет температуру плавлении, заставляющую предполагать, что она может быть идентична с туевой кислотой; температура плавления другой кислоты практически совпадает с температурой плавления чаминовой кислоты, тогда как точка кипения жидкой кислоты совпадает с точкой кипения чамовой кислоты. [26]
У кислот нормального строения наблюдается интересная закономерность: при общем повышении температуры кипения с увеличением числа углеродных атомов температуры плавления кислот с четным числом углеродных атомов выше, чем температуры плавления соседних кислот с нечетным числом углеродных атомов. [27]
С повышением молекулярной массы кислот повышается их температура кипения и понижается плотность. Температуры плавления кислот проявляют те же закономерности, что и в ряду алканов. [28]
Растворимость пропилкамфорной кислоты при 15 С равна 0 0192 г в 100 мл воды. Температура плавления кислоты, перекристаллизованной из горячей воды, 189 5 - 190 С ( резко) с выделением воды и образованием ангидрида. [29]
Растворимость пропилкамфорной кислоты при 15 равна 0 0192 г в 100 мл воды. Температура плавления кислоты, перекристаллизованиой из горячей воды, 189 5 - 190 ( резко) с выделением воды и образованием ангидрида. [30]
Страницы: 1 2 3 4