Температура - проведение - реакция
Cтраница 3
В опытах с повышенным содержанием метана в реакционной смеси при работе с воздухом и в опытах с кислородо-аргоновыми смесями максимальный выход формальдегида не был достигнут, так как ограниченная мощность источника питания плазмотрона не позволила поднять температуру проведения реакции. [31]
Для получения углеводорода без примеси галоида всегда следует брать избыток цинкорганического соединения. Температура проведения реакции должна быть по возможности низкой. Для реакции обязательно прибавление к цинкорганическо-му соединению вначале небольших порций галоидного алкила и нагревание. Минимальная температура, при которой начинается процесс, поддерживается в продолжении всей реакции. [32]
Таким образом, в данном случае при концентрациях кислорода в смеси - 40 - 45 % скорость реакции становится настолько большой, что за время нахождения в зоне реакции ( - Ю-5 сек. С увеличением температуры проведения реакции уменьшается величина концентрации кислорода, с которой начинается резкое понижение выхода формальдегида. [34]
Все эти методы основаны на свойствах совместной растворимости солей в соответствующих системах. Оптимальные концентрации и температуры проведения реакций обменного разложения подбираются по диаграммам растворимости. Во всех приведенных реакциях из образующейся пары солей хлористый аммоний остается в растворе, а вторая соль выпадает в виде кристаллов. После ее отделения хлористый аммоний выделяется из раствора кристаллизацией при охлаждении, а иногда выпариванием. [35]
Методами хромато-масс-спектрометрии и масс-спектрометрии идентифицированы промежуточные и побочные продукты, образующиеся на отдельных стадиях синтеза мономера 4 4 -дихлордифенилсульфона. Рассмотрено влияние катализатора, времени и температуры проведения реакции на образование примесей и величину выхода мо-номера. [36]
Методами хромато-масс-спектрометрии и масс-спектрометрии идентифицированы промежуточные и побочные продукты, образующиеся на отдельных стадиях синтеза мономера 4 4 -дихлордифенилсульфона. Рассмотрено влияние катализатора, времени и температуры проведения реакции на образование примесей и величину выхода мо-ломера. [37]
Поскольку рабочие температуры процесса превышают температуру плавления натрия, его можно вводить как в твердом, так и в жидком виде, что делает натрий очень удобным сокатализатором. Для поддержания растворителя в жидком состоянии при температурах проведения реакции и для поддержания необходимого парциального давления этилена процесс проводят при общем давлении порядка 1ОО атм. [38]
Поскольку рабочие температуры процесса превышают температуру плавления натрия, его можно вводить как в твердом, так и в жидком виде, что делает натрий очень удобным сокатализатором. Для поддержания растворителя в жидком состоянии при температурах проведения реакции и для поддержания необходимого парциального давления этилена процесс проводят при об-шем давлении порядка 1ОО атм. [39]
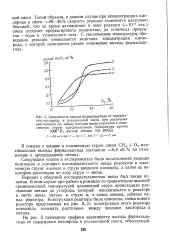
На рис. 6, а представлены результаты опытов по окислению метана кислородом воздуха в реакторе с последовательным вводом в плазменную струю воздуха и метана. На этом рисунке показаны графики зависимости выхода формальдегида от температуры проведения реакции при различных соотношениях воздуха и метана в реакционной смеси. Сплошные кривые на этом рисунке соответствуют режимам работы с охлаждением отходящих газов в теплообменнике, пунктирные - с применением закалки холодным азотом, расход которого равнялся общему расходу отходящих газов. [40]
В работе приведены результаты изучения реакций алкилирования уксусной кислоты этиленом в паровой фазе в присутствии кислых катализаторов. Термодинамический расчет реакций показал, что для увеличения выхода этнлацетата необходимо уменьшить температуру проведения реакции и увеличивать мольное соотношение этилен: уксусная кислота. Изучение влияния ряда факторов на реакцию позволило выбрать условия, в которых конверсия уксусной кислоты составляет 65 % при 100 % - ной селективности. [41]
Предельную концентрацию о тработанной серной кислоты, выраженную в процентах SO3, называют я сульфирования. Даже для одного и того же соединения она не строго постоянна: несколько падает с повышением температуры проведения реакции и зависит от исходного соотношения реагентов. Поэтому я сульфирования нельзя использовать для строгой оценки реакционной способности соединений, однако для практических задач этой величиной пользуются часто. [42]
Реакция бромбензола с енолят-ионами пинаколина в ТГФ-при фотоинициировании не дала никаких продуктов замещения ( время облучения 1 3 ч, 35 С) [46], а 2-бромпиридин взаимодействовал с енолят-ионами ацетона в условиях фотоинициирования, давая за 3 ч в ТГФ продукт замещения с выходом 64 %, Далее, 2-хлорхинолин реагировал в ТГФ, приводя к продукту замещения с тем же выходом, что и в аммиаке. Поскольку реакция в темноте осуществляется, вероятно, по термически индуцированному механизму SRN1, различия в реакционной способности могут быть отнесены на счет разницы в температуре проведения реакции, которая составляет 50 - 60 С. [43]
Оптимальные условия температуры и давления должны опреде-л ться кинетическими и каталитическими факторами, которые можно предсказать заранее лишь качественно. Так как скорости всех реакций возрастают с температурой и в то же время повышение температуры не благоприятствует образованию бутана, то можно было бы предположить, что чем выше температура проведения реакции, тем лучше идет превращение в бутадиен. С другой стороны, вследствие большой термической неустойчивости бутадиена следует ожидать, что чем ниже температура, тем меньше идет деструктивный крекинг бутадиена на водород и углерод. Следовательно, для того чтобы осуществить наиболее выгодно процесс превращения бутена в бутадиен нужно наиболее экономично сбалансировать эти два противоположно действующих фактора. Кроме того, поскольку скорость крекинга бутадиена возрастает с его концентрацией, низкая степень превращения за один прогон через конвертор даст, вероятно, больший выход бутадиена на превращенный бутен. Единственно, что кажется вполне очевидным, это преимущество процесса, идущего при низком давлении, по сравнению с процессом, осуществляемым под атмосферным или повышенным давлением. Понижение давления, безусловно, будет затруднять образование бутана и полимеризацию бутена. [44]
Вообще характер заместителей при двойной связи и условия проведения опытов, как видно из изложенного выше, существенно влияют на состав продуктов реакции. Так, гидрохлорирование 2 3-диметилбутадиена - 1 3, газообразным НС1 приводит к образованию смеси продуктов 1 4 - и 1 2-присоединения, причем выход продукта 1 4-присоединения ( 1-хлор - 2 3-диметилбутена - 2) сильно зависит от температуры проведения реакции. Оптимальный выход этого изомера ( 15 % от суммы изомеров) получен при - 69 С. [45]
Страницы: 1 2 3 4