Температура - идеальный газ
Cтраница 3
При адиабатическом процессе, согласно уравнению ( VII, 25), температура идеального газа изменяется только в том случае, если газ совершает объемную работу. Этот вывод читатели уже знают из анализа опыта Гей-Люссака. [31]
Температура реального газа в условиях свободной конвекции ( шв 0) опускается ниже температуры идеального газа за счет эффекта Джоуля-Томсона. При этом для условий Средней Азии температура реального газа возрастает с расстоянием, а для Крайнего Севера - падает. В первом случае солнечная радиация преобладает над теплоотдачей газопровода во внешнюю среду; во втором - распределение температур газа полностью определяется теплообменом с окружающим воздухом. [32]
Из уравнения ( VII, 25) следует, что при адиабатическом процессе температура идеального газа изменяется только в том случае, если газ совершает работу, - вывод, который читатели уже знают из анализа опыта Гей-Люссака. [33]
Это уравнение представляет нам ту связь, которая соединяет объем, да-вленпе и температуру идеального газа при любых их изменениях. [34]
Из уравнения ( 7 - 61) следует, что уменьшение давления на изоэнтропе приводит к понижению температуры идеального газа. Что же касается реального газа, то из уравнения ( 7 - 59) очевидно, что, поскольку всегда с О, то и в подавляющем большинстве случаев ( dv / dT) p 0, интеграл, стоящий в правой части этого уравнения, положителен, следовательно, если рг pz, той Т1 7V Таким образом, при изоэнтропном ( обратимом адиабатном) расширении вещество охлаждается. Как мы увидим в дальнейшем, процесс обратимого адиабатного расширения используется как эффективный способ охлаждения газа. [35]
В то время как при адиабатическом расширении любого газа, происходящем с совершением внешней работы, его температура сильно меняется, температура идеального газа при расширении без совершения внешней работы остается постоянной в течение всего процесса. Однако опыт показывает, что при адиабатическом расширении без совершения внешней работы температура реальных газов хотя и незначительна, но снижается; снижение его происходит за счет работы внутримолекулярных, так называемых ван-дер-ваальсовых, сил. [36]
При этом температура газа будет возрастать в соответствии с увеличением его внутренней энергии [ см. (18.17) j, откуда следует, что температура идеального газа пропорциональна его внутренней энергии. Давление газа р также будет возрастать пропорционально температуре. [37]
При дросселировании идеального газа fe - i cp ( t2 - i) 0, поэтому tyU, откуда следует, что температура идеального газа при дросселировании не меняется. При дросселировании реальных газов и паров температура может увеличиваться, уменьшаться и оставаться неизменной. Понижение температуры реального газа при адиабатном дросселировании называется п о-ложительным эффектом Джоуля-Томсона, а повышение - отрицательным эффектом. [38]
Так как гравитационное поле не влияет на распределение молекул по скоростям, оно не влияет также и на среднюю кинетическую энергию молекулы, а следовательно, и на температуру, так как температура идеального газа пропорциональна средней кинетической энергии молекулы. В равновесных условиях при отсутствии иных внешних воздействий, кроме поля, температура газа должна быть одинакова на всех высотах. [39]
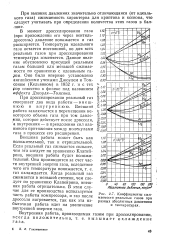 |
Коэффициенты сжимаемости реальных газов при разных абсолютных давлениях и температурах. [40] |
В момент дросселирования газа ( при прохождении его через вентиль-дроссель) давление понижается и газ расширяется. Температура идеального газа остается постоянной, но для всех реальных газов при дросселировании температура изменяется. Данное явление обусловлено присущей реальным газам большей или меньшей сжимаемости по сравнению с идеальным га - ом. Оно было впервые установлено английскими учеными Джоулем и Том-соном ( Кельвином) в 1852 г. и с тех flop известно в физике под названием аффекта Джоуля-Томсона. [41]
Теплоемкость Cv отлична от нуля, и dT равно нулю. Температура идеального газа, совершившего бесконечно малый процесс Гей-Люссака, не должна измениться. [42]
Так, любое увеличение фазового пространства, доступного молекуле данной системы, отражается на увеличении энтропии. Если температура идеального газа увеличивается без изменения занятого газом объема, энтропия возрастает, так как для молекулы становится доступной большая область пространства импульсов. И в этом случае можно при помощи статистической механики показать, что энтропия измеряется частным от деления количества поглощенного тепла, приходящегося на одну молекулу, на температуру. Молекулярная энтропия, будучи мерой фазового пространства, доступного частицам системы, зависит только от состояния системы, и отношение ее к теплоте, поглощенной в любом механически обратимом процессе, является сущностью второго закона термодинамики. [43]
 |
Изображение процесса дросселирования в различных системах координат. [44] |
Следовательно, процесс дросселирования проводится по изоэнталь-i пе. Изменений температуры идеального газа не происходит ( Т1 Т2), так как энтальпия идеального газа не зависит от давления. [45]
Страницы: 1 2 3 4