Температура - идеальный газ
Cтраница 4
До сих пор квантовому рассмотрению подвергались лишь колебательные и ( иногда) вращательные степени свободы частиц. Однако, если температура идеального газа ( при заданной его плотности) достаточно мала, то для всех степеней свободы, в том числе и поступательных, плотность одночастичных квантовых состояний не будет малой и возникнет квантовомеханическое обменное взаимодействие. Изучение газов при низких температурах, к которому мы переходим, должно, следовательно, быть с самого начала квантовым. Мы ограничимся идеальными квантовыми газами, в которых пренебрегается обычным силовым взаимодействием частиц. [46]
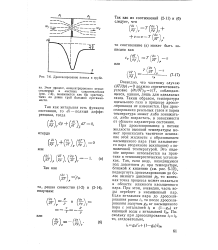 |
Дросселирование потока в трубе. [47] |
Очевидно, что частному случаю ( дТ / др) г 0 должно соответствовать условие ( dv / dT) pv / T, соблюдающееся, однако, лишь для идеальных газов. Таким образом, температура идеального газа в процессе дросселирования не изменяется. При дросселировании реальных газов и паров температура может либо понижаться, либо возрастать, в зависимости от области параметров состояния. [48]
Внутренняя энергия идеального газа прямо пропорциональна его абсолютной температуре. Следовательно, при изменении температуры идеального газа обязательно изменяется его внутренняя энергия; если температура остается постоянной, то внутренняя энергия идеального газа не изменяется. [49]
Внутренняя энергия и, следовательно, температура идеального газа при расширении его в пустоту остаются постоянными. [50]
Значит, в процессе Джоуля - Томсона температура идеального газа остается неизменной. [51]
Сравнение теоретических и экспериментальных данных показывает, что выведенные формулы удовлетворительно соответствуют течению реального газа в скважине. Для сравнения на рис. III.7 нанесены кривые распределения температур идеального газа. Вследствие термодинамической неидеальности температура реального газа становится ниже, чем идеального. [52]
Сравнение теоретических и экспериментальных данных показывает, что выведенные формулы удовлетворительно описывают поведение реального газа при течении его в скважине. Для сравнения на рис. 2 нанесены кривые распределения температур идеального газа. Из рис. 2 видно, что за счет термодинамической неидеалъности температура реального газа становится ниже, чем идеального. [53]
 |
Дросселирование потока газа. [54] |
Для идеальных газов коэффициент D - равен нулю. Это означает, что при неизменном уровне энтальпии ( i const) сохраняет неизменную величину и температура идеального газа ( t const), независимо от изменения давления газа. [55]
Ранее, в § 2 - 4, мы рассмотрели этот процесс применительно к идеальному газу. Напомним, что экспериментальное изучение процесса адиабатного расширения без отдачи внешней работы газа, близкого к идеальному, позволило Гей-Люссаку, а затем Джоулю установить, что температура идеального газа в результате этого процесса не изменяется; это в свою очередь позволило установить важное свойство идеального газа - независимость внутренней энергии от объема. [56]
Для этого давление газа на стадии сжатия должно быть меньше, чем на соответствующей стадии расширения. С понижением температуры давление данной массы газа также понижается, если при этом не изменяется ее объем. Соотношение между давлением, объемом и температурой идеального газа описывается объединенным газовым законом. [57]
Рассмотрим, прежде всего, эффект Джоуля - Томсона в идеальном газе. Для идеального газа внутренняя энергия U является функцией одной только температуры. Произведение PV равно RT и тоже зависит только от температуры. Поэтому и энтальпия идеального газа зависит от одной только температуры. При процессе Джоуля - Томсона энтальпия, а значит и температура идеального газа, не меняется. Поэтому, как уже указывалось, изменение температуры и является чувствительным индикатором, указывающим на отличие реальных газов от идеального. [58]
Страницы: 1 2 3 4