Температура - дегидратация
Cтраница 1
Температуры дегидратации ( выделение гидроксильных групп) также ложатся на непрерывную кривую с температурой разложения чистого конечного члена гросеуляра около 1000 С. Диаграммы давление - температура, построенные по данным гидротермальных экспериментов Иодера, приведены на фиг. [1]
Температура дегидратации гипса несколько зависит от его структуры. [2]
Температура дегидратации стехиометрических гидроксилсодержащих соединений лантаноидов ( Ln ( OH) 3 и LnOOH) зависит, с одной стороны, от их природы, а с другой, от свойств и условий получения. [3]
Температура дегидратации стехиометрических гидроксилсодер-жащих соединений лантаноидов ( Ln ( ОН) 3 и LnOOH) зависит, с одной стороны, от их природы, а с другой, от свойств и условий получения. [4]
Если температура дегидратации понижается по ряду La - Lu - KgLnX2; KsLnZ3, то эта вода - внешнесферная. В обратном случае ( LnECl, LnEOH) - внутрисферная. [5]
Определены температуры дегидратации, плавления, разложения, полиморфных превращений. [6]
Повышение температуры дегидратации действительно приводит к появлению этилена. При 450 С и 120 атм давления наступает химическое равновесие с системой спирт - эфир - этилен - вода. Таким образом, картина химического процесса становится значительно более ясной. [7]
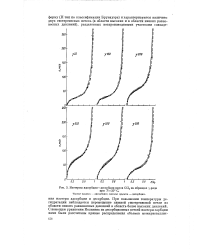 |
Изотермы адсорбции-десорбции паров CCL на образцах у-ряда. [8] |
При повышении температуры дегидратации наблюдается перемещение нижней гистерезисной петли из области низких равновесных давлений в область более высоких давлений. [9]
С повышением температуры дегидратации окиси кремния достигается максимальное удаление остаточных гидроксильных групп с поверхности носителя. [10]
Показано, что температура дегидратации должна рассматриваться как один из определявдих факторов при разработке технологии приготовления рабочих растворов неионогенных деемульга-торов и как фактор для выбора температурного режима деэмульса-ции. [11]
Термогравиметрическим методом определены температуры дегидратации и разложения полученных комплексов. [12]
Иными словами, температура дегидратации последних тем ниже, чем сильнее поляризующее действие катиона и менее прочна ионная связь металл - гидроксил. [13]
Оказалось [13], что температура дегидратации CdBr2 - 4H2O повышается от 35 5 С при атмосферном давлении до 67 0 С при давлении 9 кбар. [14]
Согласно термогравиметрическим исследованиям [41 ] температура дегидратации Ni ( ОН) 2 несколько зависит от условий осаждения. После потери вначале небольшого количества адсорбированной воды в интервале от 100 - 115 до 250 - 260 С дальше начинается разложение гидроокиси, которое практически заканчивается при 500 - 530 С. Максимальная убыль в весе образцов происходит примерно около 330 С. Установлено [300], что гидроокись никеля ( II), полученная из растворов NiSO4 и NaOH, теряет воду, превращаясь в NiO при давлении 80 кбар и температуре 344 10 С. [15]
Страницы: 1 2 3 4