Температура - детонация
Cтраница 1
Температура детонации, напротив, зависит от этого распределения гораздо сильнее. [1]
В результате дополнительного поглощения энергии, расходуемой на увеличение диссоциации, температура детонации при избытке кислорода понижается, что и приводит к уменьшению скорости детонации. [2]
Аналогичные расчеты для гремучего газа с добавками других газов и с учетом степени диссоциации продуктов взрыва при температуре детонации Тц приведены в табл. 5.2. Из таблицы видно, что скорость детонации газовой смеси существенно зависит от природы добавляемого газа. Добавка азота и кислорода снижает скорость детонации. Добавка же Н2 приводит к значительному повышению скорости детонации, несмотря на то, что температура детонирующей смеси при этом заметно падает. Эти факты хорошо согласуются с теорией. [3]
Кук обратил внимание на то, что из всех параметров, характеризующих детонацию в конденсированных системах, только температура детонации позволяет судить о точности применяемых на практике уравнений состояния. [4]
 |
Зависимость скорости детонации в ацетилено-ки-слородных смесях от состава. [5] |
Аналогичная картина наблюдается также в случае детонации смесей C3N2, 02 и N2, где увеличение скорости и температуры детонации при замене кислорода азотом объясняется происходящим при этом уменьшением степени диссоциации кислорода. Так, при переходе от смеси C2N2 302 к смеси C2N2 02 2N2, согласно вычислениям Зельдовича ] 117 ], скорость и температура детонации увеличиваются соответственно от 2135 до 2265 м / сек и от 4095 до 4395 К. Измеренные значения скорости детонации равны: для первой смеси 2110 м / сек ( Диксон), для второй смеси 2165 м / сек. [6]
 |
Расчет D по методу И. Н. Аи. [7] |
Здесь ( Звзр - теплота взрыва, определяемая по (6.9); Су - суммарная теплоемкость продуктов взрыва; Тн - температура детонации; Мср - средняя молекулярная масса газообразных ПВ, г / моль. [8]
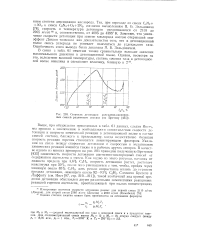 |
Скорость детонации ацетилсно-кислород-ных смесей различного состава ( по Бретону. [9] |
Так, при переходе от смеси ЗО2 к смеси C2N2 O2 2N2, согласно вычислениям Я. Б. Зельдовича [78], скорость и температура детонации увеличиваются от 2135 до 2265 м / сек 86 и, соответственно, от 4095 до 4395 К. Заметили, что увеличение скорости детонации при замене кислорода азотом открывший этот эффект Диксон толковал как доказательство того, что в детонационной волне окись углерода не успевает окислиться до углекислого газа. [10]
Более подробные вычисления, в которых учитывались сжимаемость и теплопроводность наполнителя и пренебрегалось увлечением инертных частиц [16, 17], показывают, что такого рода добавки могут понизить температуру детонации на-500 С. В этом случае длительность периода выделения энергии определяется скоростью протекания процессов, нечувствительных к изменению температуры, например процесса газификации взрывчатого вещества и процесса диффузии радикалов в направлении к частицам, с которыми они вступают в окончательную реакцию. Важная роль, которую играет размер зерна при определении характеристик выделения энергии в процессе детонации твердых веществ, подчеркивается также влиянием, которое он оказывает на такие свойства, как чувствительность к удару и затухание. [11]
 |
Концентрационные пределы детонации пропа-но-кислородных смесей. [12] |
В табл. 35 обращают на себя внимание также высокие значения максимальной температуры детонации ТГ, значительно превышающие максимальные температуры нормального горения. В этом случае температура детонации, по оценке Михельсона и Зельдовича ( см. [117]), превышает 6000 К, а температура нормального горения, по вычислениям Гейдона и Вольфгарда [827], составляет 4850 К. Как уже указывалось выше, причиной более сильного разогрева газа в детонационной волне является сжатие газа потоком отходящих горячих газов. [13]
Планка; k - постоянная Больцмана; р - давление газа; Wi - энергия ионизации атомов газа; Т - абсолютная температура. Не удается установить связь и с температурой детонации. В частности, в азиде свинца и в ТНТ обнаруживается более высокая проводимость, чем в ТЭНе, температура детонации которого значительно выше. [14]
Из табл. 61, далее, видна высокая степень диссоциации газов в детонационной волне, откуда следует необходимость учета этого эффекта при вычислениях скорости детонации, на что также указывалось выше ( стр. Как видно из табл. 61, различие скоростей и температур детонации при эквивалентной замене кислорода азотом должно быть обусловлено главным образом различием в степени диссоциации смесей. [15]
Страницы: 1 2