Низкая температура - окисление
Cтраница 1
Низкие температуры окисления в термокаталитическом процессе ( 200 - 500 С в зависимости от природы окисляемой примеси и типа катализатора) обусловливают снижение расхода топлива по сравнению с термическим способом в 2 - 3 раза. [1]
Низкие температуры окисления в термокаталитическом процессе ( 200 - 500 С в зависимости от природы окисляемой примеси и типа катализатора) обусловливают снижение расхода топлива по сравнению с термическим способом в 2 - 3 раза. Термокаталитическому окислению могут подвергаться как индивидуальные компоненты, так и смеси углеводородов или кислородсодержащих органических веществ. Средний срок службы катализаторов в процессах очистки отходящих газов составляет 3 - 5 лет при отсутствии в газах катализаторных ядов. [2]
Низкие температуры окисления в жидкой фазе способствуют развитию реакций полимеризации и конденсации. Реакции перокси - дации и распада протекают в незначительной степени. Поэтому углеводороды, окисляющиеся при нормальных температурах, в основном образуют кислородные соединения и смолистые вещества с большим молекулярным весом, чем у исходных углеводородов. [3]
Таким образом, при низкой температуре окисления в отсутствие разветвления цепей, взаимодействия ингибиторов с перекисью и инги-биторных радикалов с углеводородом, то есть в отсутствие продолжения цепи, усиление эффективности может вызываться только переносом водорода от шенола к амину. [4]
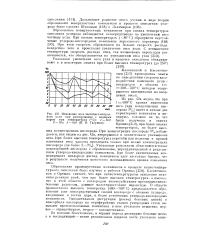 |
Изменение веса частицы электродного угля при реагировании с водяным паром при температурах ( С. 1 - 500. 2 - 550. 3 - 600 ( П. Н. Галушко. [5] |
Образование поверхностных комплексов при низких температурах окисления углерода наблюдается непосредственно по увеличению веса частицы угля. При этом скорость образования их больше скорости распада, вследствие чего и происходит увеличение веса угля. [6]
Из этих рисунков следует, что даже при низких температурах окисления, начиная от 125, через определенное время в результате поглощения кислорода достигается максимум на кривой изменения веса. При всех трех температурах, особенно при наиболее высокой, и прежде всего у молодых углей после короткого периода инициирования наступает некоторое уменьшение содержания углерода и водорода. [7]
Рассматривая распределение углерода окисленного керогена по продуктам окисления ( табл. 3), следует обратить внимание на следующее: при низкой температуре окисления ( 100) с увеличением рабочего давления и, следовательно, парциального давления кислорода возрастает количество углерода окисленного керогена, израсходованного на образование высокомолекулярных, двухосновных и среднемолекулярных кислот при одновременно меньших затратах углерода окисленной органической массы на образование углекислоты. [8]
В данном случае используется цепь термоэлементов, заключенная в устойчивый к коррозии, действующий как катализатор керамический материал, который в сравнении с платиновой спиралью эффективен даже при низких температурах окисления. Смещение точки нуля ограничено благодаря эталонной оценке измерений, по некаталитической субстанции. Полная настройка измерительных устройств производится при постоянной температуре в реакционной камере. [9]
В большинстве случаев керосины, содержащие серу в виде различных органических соединений, будучи подвергнуты окислению ( в особенности при высоких температурах), лишь осмо-ляются и выделяют липкие шламообразные осадки некислого характера. При низких температурах окисления порядка 120 - 135 С в составе керосиновых фракций, содержащих серу, вообще не наблюдается каких-либо изменений. [10]
Они показали, что в зависимости от температуры окисления кислород воздуха может расходоваться по-разному. Причем при низких температурах окисления ( до 200 - 250 С) в основном происходит образование сложно-эфирных связей, а при температуре выше 200 - 250 - G начинает преобладать образование связей С-С - за счет реакций дегидрирования. Поэтому в первом случае происходит накопление кислорода в битуме в процессе окисления, а во втором этого не происходит. [11]
 |
Кинетика окисления крем - ния xsio2 - f ( t в сухом кислороде при различных температурах. [12] |
Если коэффициент преобразования примеси т 1 ( в случае фосфора), то примесь в основном ускоряет химическую реакцию на поверхности раздела и кинетика роста оксида подчиняется параболическому закону. Это наиболее ярко проявляется при низких температурах окисления. [13]
Вероятно, синергизм действия смеси амина и сульфида объясняется тем, что первый компонент при обрыве цепи окисления образует гидропероксидную группу ( см. выше), а второй разрушает ее, увеличивая время жизни первого компонента ( амина), поскольку уменьшается число окислительных цепей. Амины и фенолы более эффективны при низких температурах окисления, а превентивные антиоксиданты - при высоких. [14]
Вероятно, синергизм действия смеси амина и сульфида объясняется тем, что первый компонент при обрыве цепи окисления дает молекулу гидроперекиси ( см. выше), а второй разрушает ее, увеличивая время жизни первого компонента ( амина), поскольку уменьшается число окислительных цепей. Амины и фенолы более эффективны при низких температурах окисления, а превентивные антиоксиданты - при высоких. [15]
Страницы: 1 2