Равновесная температура
Cтраница 3
Равновесная температура фазового перехода низкотемпературной модификации II составляет 80 С, а температура плавления модификации I близка к 130 С. [31]
Равновесную температуру называют температурой начала реакции. Она позволяет судить о начале развития реакции в желаемом направлении. [32]
Если равновесная температура определена точно, то значение переменной SUMX1 равно нулю с заданной точностью и управление передается метке 650, где вызывается подпрограмма вывода конечных результатов. Если для расчета ви-риальных коэффициентов было использовано разложение в ряд по давлению, соответствующая информация об этом печатается. После вывода программа передает управление оператору с меткой 520 для чтения следующей карты исходной информации. [33]
Зависимость равновесной температуры от входнойу0 для случая, когда в системе возможно несколько состояний равновесия, имеет гис-терезисный характер. Переход с участка кривой 05 на участок кривой DE осуществляется в точке бифуркации В при у Уо11 - При обратном движении, т.е. при уменьшении у0, мы будем двигаться сначала по участку. [34]
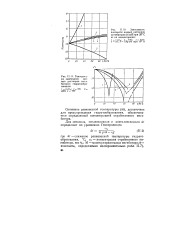 |
Зависимость плотности водных растворов ингибиторов ( г / см8 при 20 С эт их концентрации.| Температура замерзания водных растворов ипги-биторов гидратообра-зования. [35] |
Снижение равновесной температуры ( Д /), достаточное для предупреждения гидратообразования, обеспечивается определенной концентрацией отработанного ингибитора. [36]
Снижение равновесной температуры ( см. рис. 51) гидратообразования при наличии в системе углеводородного растворителя объясняется растворением в ней части пропановых фракций газа. Эти фракции имеют более высокую температуру гидратообразования. При наличии пироконденсата образуются очень рыхлые гидраты и плохо удерживаются на стенках. Таким образом, пироконденсат препятствует контакту газа с водой, поэтому заметно уменьшается образование кристаллов гидрата. Полученные рыхлые гидраты свободно уносятся потоком газа и образование гидратных пробок полностью предотвращается. [37]
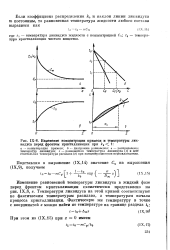 |
Изменение концентрации примеси и температуры ликвидуса перед фронтом кристаллизации при ka 1. [38] |
Изменение равновесной температуры ликвидуса в жидкой фазе перед фронтом кристаллизации схематически представлено на рис. IX, 8, в. Температуры ликвидуса на этой кривой соответствуют не фактическим температурам расплава, а температурам начала процесса кристаллизации. [39]
Определим равновесную температуру и относительную влажность камер хранения холодильника до реконструкции для работы батарей по затопленному варианту с жидкостным отделителем. [40]
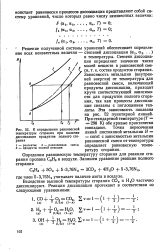 |
К определению равновесной температуры сгорания при наличии диссоциации продуктов полного сгорания. [41] |
Определим равновесную температуру сгорания для реакции сгорания пропана С3Н8 в воздухе. [42]
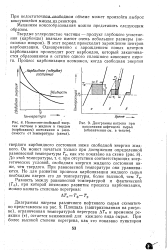 |
Изменение свободной энергии системы в жидком и твердом ( карбоидном состояниях в зависимости от температуры ( схема.| Диаграммы нагрева при. [43] |
При равновесной температуре они уравниваются. [44]
При равновесной температуре 7 величины свободных энергий металла в жидком и твердом состояниях равны; металл в обоих состояниях находится в равновесии. Выше Ts более устойчив жидкий металл, имеющий меньший запас свободной энергии, а ниже этой температуры устойчив твердый металл. [45]
Страницы: 1 2 3 4 5