Теплота - нейтрализация
Cтраница 1
Теплоты нейтрализации прочих гидроксилпроизводных, не приведенных в табл. 14, можно находить, пользуясь аналогиями и руководствуясь вышеизложенными основными положениями, с учетом всех тех факторов, которые могут оказать влияние на величину теплоты нейтрализации. [1]
Теплоты нейтрализации соляной и уксусной кислот едким натром соответственно равны 13 75 и 13 3 ккал г-экв. Вычислить диссоциацию уксусной кислоты, если ее рассматривать в водном растворе практически совершенно недиссоциированной. [2]
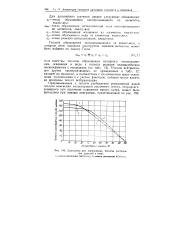 |
Диаграмма для определения теплоты растворения щелочей в поде. / - теплота растворения NaOH ( тв.. 2-теплота растворения КОН ( тв... [3] |
Теплоты нейтрализации других оксипроизводных, не приведенных в табл. 12, находят по аналогии, в соответствии с изложенными выше основными положениями и с учетом факторов, которые могут влиять на величины теплот нейтрализации. [4]
Теплота нейтрализации представляет собой количество тепла, выделяющееся при нейтрализации 1 г-экв кислоты 1 г-экв щелочи. [5]
Теплота нейтрализации - это то количество теплоты, которое выделяется при нейтрализации грамм-эквивалента кислоты грамм-эквивалентом основания. Теплоты нейтрализации сильных кислот сильными основаниями близки между собой и в среднем равны 13 6 ккал / г-экв. G-точки зрения теории электролитической диссоциации сущность реакции нейтрализации состоит во взаимодействии между катионом водорода ( носителем кислотных свойств) и ионом гидрокснла ( носителем основных свойств) с образованием малодиссоциирующей воды. [6]
Теплота нейтрализации НС1 составляет - 56 6, а борной кислоты - 42 7 кДж / моль. [7]
Теплоты нейтрализации соляной, уксусной и масляной кислот гидроксидом натрия соответственно равны - 55 9; - 56 07 и - 57 74 кДж / моль. Какова теплота диссоциации уксусной и масляной кислот, если они в водном растворе практически не диссоциируют. [8]
Теплота нейтрализации составляет ( по данным теплового баланса) 815 000 кдж на одну операцию, а так как процесс длится 2 часа, то тепловая нагрузка будет 0113 кет. [9]
Теплоты нейтрализации соляной, уксусной и масляной кислот едким натром соответственно равны - 55 9; - 56 07 и - 57 74 кдж / моль. Какова теплота диссоциации уксусной и масляной кислот, если они в водном растворе практически не диссоциируют. [10]
Теплота нейтрализации 1 моля едкого натра 1 молем азотной кислоты равна - 13 660, а 1 модем дихдоруксусной кислоты равна - 14 830 ккал / моль. [11]
Теплота нейтрализации, следовательно, определяется в данном случае теплотой образования молекул воды и ионов водорода и гидроксила в растворе. [12]
Теплота нейтрализации равна количеству теплоты, выделяющейся при нейтрализации 1 г-экв кислоты 1 г-экв щелочи. [13]
Теплота нейтрализации - тепловая энергия, выделяемая при нейтрализации 1 моль ионов водорода в кислом растворе каким-либо основанием, если реакция протекает в разбавленном водном растворе. В реакциях между сильными кислотами и сильными основаниями оба реагента полностью ионизированы и реакция протекает между 1 моль ионов водорода и 1 моль гидроксид-ионов. Для слабых кислот или слабых оснований выделяемая тепловая энергия меньше 57 3 кДж, поскольку часть выделяемой энергии используется для того, чтобы ионизация кислоты или основания стала полной. [14]
Теплота нейтрализации, считая на граммолекулу, составляет для азотной кислоты 13500 кал, а для серной 31 380 кал. Если же теплоту нейтрализации этих кислот считать на моль щелочи, на-пример NaOH, пошедшей на нейтрализацию, то величина ее для обеих кислот оказывается довольно близкой: 13500 кал для азотной и 15680 кал для серной. [15]
Страницы: 1 2 3 4