Анилиний
Cтраница 3
В связи со слабой кислотностью аминов, для оценки влияния групп на кислотные свойства аминов в настоящее время часто определяют константы ионизации аммониевых ионов, в частности, например, иона анилиния. [31]
Окрашенное соединение, соответствующее нейтральному парарозанилину, можно наблюдать в связи с тем, что значение его рКа слишком мало, чтобы в условиях эксперимента могла образоваться бесцветная соль, подобная соли анилиния. [32]
В этом синтезе нитрование ацетанилида имеет преимущество перед нитрованием самого анилина не только потому, что анилин легко окисляется азотной кислотой, но и вследствие того, что реакция с анилином приводит к значительному желш-замеще-нию в образующемся ионе анилиния. Еще один путь, приводящий к n - нитроанилину, заключается в нитровании хлорбензола и последующем замещении хлора на аминогруппу при действии аммиака. [33]
В случае солей фенилоксония PhOH2, как показывают квантово-химические расчеты с учетом всех валентных электронов [111], - f - M-эффект оксониевого кислорода не проявляется, и распределение электронной плотности в бензольном кольце близко к найденному для иона анилиния. [34]
В этом синтезе нитрование ацетанилида имеет преимущество перед нитрованием самого анилина не только потому, что анилин легко окисляется азотной кислотой, но и вследствие того, что реакция с анилином приводит к значительному жета-замещению в образующемся ионе анилиния. Еще один путь, приводящий к w - нитроанилину, заключается в нитровании хлорбензола и последующем замещении хлора на аминогруппу при действии аммиака. [35]
LXII) и C6H5CR R C1 ( LXIII) должны изменяться аналогично основ-ностям аминов, получаемых замещением СС1 на N, так как те же факторы, которые влияют на ионизацию этих производных бен-зилхлорида, будут влиять и на диссоциацию ионов анилиния. [36]
 |
Кривые титрования 0 10 М растворов слабых оснований. аммиака ( рКа 9 2, триэтаноламина ( рКа 7 8 и пиридина ( рКа 5 3 раствором сильной кислоты НС1. [37] |
Он является недостаточно сильным основанием, для того чтобы его можно было титровать кислотой. Однако ион анилиния представляет собой уже настолько сильную кислоту, что его можно титровать раствором сильного основания. [38]
Ацилирование аминогруппы уничтожает ее ауксохромный характер; вследствие сопряжения, представленного VIII, или таутомерии IX, неподеленная пара электронов атома азота теряет способность участвовать в сопряжении с ядром с образованием полярных структур типа VII. В отличие от иона анилиния, спектр поглощения которого почти идентичен спектру поглощения бензола, бензанилид поглощает в области более длинных волн, чем бензол. [39]
Ароматические амины имеют пониженную основность вследствие мезо-мерного эффекта, благодаря которому амин как сопряженное основание иона анилиния в большей степени стабилизирован. Этим объясняется повышенная кислотность иона анилиния и низкая основность анилина по сравнению с алкиламинами, например с этиламином. [40]
Объясните, почему ион анилиния не стабилизируется вследствие резонанса, ( Примечание: попытайтесь нарисовать резонансную структуру, в которой положительный заряд находится на фенильной группе. Следует ли ожидать, что ион анилиния будет реагировать с хлорид-ионом тем же образом, что и с бензил-катионом. [41]
 |
Значения II0 для некоторых кислот и кислотных систем. [42] |
Численно НА всегда меньше Н0, и такое различие, несомненно, связано с различием в гидратации катионов. По-вндимому, амидные катионы гидратированы сильнее ионов анилиния, и поэтому образовать катион в концентрированной кислоте амиду становится труднее, чем анилину. [43]
Один из классов реакций, к которым применимы константы 0 -, включает реакции в боковой цепи ароматических соединений, в которых обычно ( но не обязательно) путем отщепления протона а-атом боковой цепи приобретает отрицательный заряд и пару электронов, которая может сопрягаться через кольцо с электроноакцепторным пара-ааместителем. К этой категории реакций относится депротонирование фенолов и ионов анилиния. Прототропная а-депро-тонизация, например, фенилнитрометана должна также относиться к этой категории реакций, хотя ( насколько это известно автору) эта область применения констант ст еще не была проиллюстрирована. Другой большой класс реакций включает бимолекулярные реакции нуклео-филыюго замещения в ароматическом ряду. Обычно считают, что эти отклонения от линейности ро - зависимости связаны с эффектами электроотрицательного сопряжения мара-заместителей. Разность о - - а, представленная в последней строке табл. 215, может соответственно рассматриваться как мера силы сопряжения заместителей - К-т-па. [44]
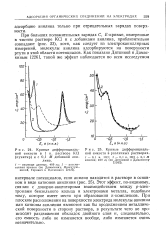 |
Кривые дифференциальной емкости в 1 н. растворе КС1 ( пунктир и с 0 1 М добавкой анилина.| Кривые дифференциальной емкости в различных растворах. [45] |
Страницы: 1 2 3 4