Теснер
Cтраница 1
Теснер [78] нашел, что энергия активации элементарного распада С2Н2 при увеличении температуры падает до нуля. Если протекание первой реакции, как и всякого фазового перехода, может быть заторможено, то вторая стадия протекает с большой скоростью и с низкой энергией активации, так как сажевые зародыши обладают, по-видимому, заметной каталитической активностью. Следует отметить, что физико-химический процесс элементарного распада ацетилена весьма сложен. [1]
Теснер рассматривает образование сажи при термическом разложении углеводородов как физико-химический процесс возникновения новой твердой фазы, подчиняющийся двум одновременно развивающимся стадиям: образованию зародышей новой фазы и их росту. Термодинамически наиболее трудной и требующей наибольшего пересыщения стадией является образование зародышей. Рост образовавшихся зародышей происходит быстро при меньшем пересыщении системы, сильным падением которого он всегда сопровождается. Скорость образования зародышей зависит от скорости пересыщения системы. [2]
Теснер и сотрудники [108, 109] в результате электронно-микроскопических наблюдений установили, что при термическом разложении углеводородов в присутствии частиц сажи отложение углерода на поверхности этих частиц происходит равномерным по толщине слоем и новых частиц не образуется. [3]
Теснером и Рафалькес [182] было найдено, что существуют минимальные ( пороговые) концентрации углеводорода при данной температуре, при которых образуются сажевые частицы. При меньших же концентрациях углеводорода сажевых частиц не образуется. [4]
Исследованиями Теснера и Рафалькес [2] показано, что продуктами распада метана на поверхности являются свободный углерод и водород. Объемное разложение метана приводит к образованию водорода и новых, более тяжелых углеводородов. [5]
Марьясин и Теснер [285] определили величину энергии активации для реакции С О2 52 ккал / моль. [6]
Марьязин и Теснер [180] исследовали кинетику роста частиц углерода при разложении метана в присутствии большого избытка водорода, который использовался в качестве газа-носителя. Предположив, что скорость зависит от концентрации метана в первой степени, эти авторы получили константы скорости в интервале температур 1400 - 1700, очень близкие к величинам, вычисленным по графику Аррениуса, а для энергии активации была найдена величина - 40 ккал. Из-за сильного замедляющего действия избытка водорода ( если в качестве газа-носителя используется гелий или азот, скорость реакции сильно возрастает) очень трудно сделать выводы относительно механизма процесса, однако полученные результаты очень полезны в практическом смысле. [7]
В работах Теснера и Тимофеевой [2] показана взаимосвязь между температурой пиролиза и глубиной заполнения пор пироуглеродом, а также изменение плотности пироуглерода, осажденного при разных температурах. [8]
Полякова, Рафалькес, Рабинович и Теснер 47 изучали взаимодействие ацетилена с парами воды проточным методом при 1200 С под атмосферным давлением. Было показано, что в рассматриваемых условиях конверсия протекает значительно медленнее, чем разложение ацетилена до элементов. Нам известна только одна работа23, в которой приводится вывод кинетических закономерностей, в частности, для окисления ацетилена водяным паром. [9]
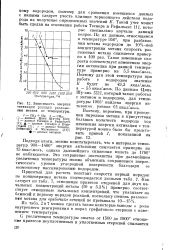 |
Зависимость энергии активации реанции разложения метана от температуры. [10] |
Такой учет может быть сделан на основании работы Теснера и Рафалькес [1], которые специально изучали данный вопрос. По их данным, относящимся к температуре 950, при разбавлении метана водородом до 10 % - ной концентрации метана скорость разложения метана снижается примерно в 100 раз. Такое изменение скорости соответствует изменению энергии активации при данной температуре примерно на 5 5 ккал / молъ, Поэтому для этой температуры при работе с водородом значение Е будет не 49 3 ккал / молъ, а - 55 ккал / молъ. [11]
Непосредственные измерения скорости разложения углеводородов на поверхности были сделаны Теснером и Рафалькес [6], однако это исследование проводилось при низких температурах ( до 800) в кинетической области. Для наших целей необходимо было определить скорости данного процесса на поверхности различных пористых контактов при температуре 1000 - 1300 в условиях переменных концентраций метана и водорода. [12]
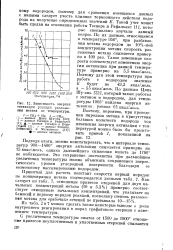 |
Зависимость энергии активации реанции разложения метана от температуры. [13] |
О - данные Цянь Шу-ань [22]; Д - данные Теснера и Рафалькес [1]; А - данные Теснера и Ечеи-сто ой [2]; х - данные Теснера, Робинович и Матюшенко [ 21J; ф - данные авторов. [14]
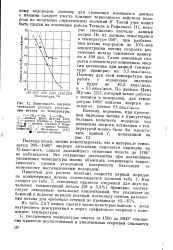 |
Зависимость энергии активации реанции разложения метана от температуры. [15] |
Страницы: 1 2