Тетрааммиакат
Cтраница 1
Тетрааммиакаты Pt ( II) и Ni ( II) имеют разную геометрическую конфигурацию, а их тетрациано-комплексы одинаковую. [1]
Тетрааммиакат сернокислой меди получается взаимодействием медного купороса CuSO4 5Н2О с аммиаком. [2]
Тетрааммиакат сернокислой меди - длинные игольчатые кри - сталлы темно-синего ( василькового) цвета. [3]
Крупные катионы тетрааммиаката меди расклинивают сильно набухшие макромолекулы за счет связывания ОН-ионов и их сильной сольватации. В результате макромолекулы большой протяженности получают возможность свободного движения в растворе и приобретают кинетическую независимость. Возникает так называемый медно-аммиачный раствор целлюлозы. Про-давливание его в кислый горячий раствор дает медно-аммиачный шелк, в котором регенерируется исходная целлюлоза, но только в другой структурной форме. [4]
Например, использование тетрааммиаката меди при сверлении а - латуни приводит к двух-трехкратному ускорению процесса сверления. [5]
Малорастворимы гекса - и тетрааммиакаты солей тяжелых металлов. [6]
Распространены следующие комплексные ионы цинка: тетрааммиакат [ Zn ( NH3) J, тетрацианат [ Zn ( CN) 4P -, тетрароданид [ Zn ( SCN) 4P и др. Хлориды, сульфаты, нитраты и ацетаты цинка растворяются в воде. [7]
Согласно Штоку [9], пентаборан-9 образует с аммиаком тетрааммиакат, устойчивый при комнатной температуре. [8]
 |
Спектры ЭПР комплексов меди с аммиаком. [9] |
Дальнейшее увеличение p [ NH3 ] приводит к уменьшению концентрации тетрааммиаката и росту концентрации сначала триаммиаката, а затем, начиная с p [ NH3 ] 2, и концентрации диаммиаката. С ростом p [ NH3 ] одновременно ухудшается разрешенность СТС, так как наложение друг на друга спектров ЭПР разных комплексов приводит к смазыванию СТС. Поскольку концентрация триаммиаката не может превысить 60 % от общей концентрации ионов меди, регистрация индивидуального спектра этого комплекса невозможна. [10]
К определенной части раствора добавляют по каплям раствор аммиака до образования тетрааммиаката меди. Следует избегать избытка аммиака. [11]
В той же таблице приведены значения произведений растворимости соответствующих гидроокисей и константы нестойкости тетрааммиакатов. Сопоставление этих данных показывает, что произведения растворимости оксинатов двухвалентных катионов значительно меньше произведений растворимости соответствующих гидроокисей, тогда как для трехвалентных катионов имеет место обратное отношение. Повидимому, в данном случае огромную роль играет способность двухвалентных катионов координировать атом азота; она достаточно хорошо характеризуется приведенными в таблице значениями констант нестойкости соответствующих тетраммино-комплексов. Для А13 и Fe3, как это указывает Эфраим, получить аммиакаты в водном растворе вообще невозможно. [12]
В решетке таких солей, как Cu ( NHs) 4SO4 - 5H2O присутствует ион тетрааммиаката меди Си ( ЫН3) Г - В растворе же некоторые из указанных ионов могут терять молекулы аммиака, другие - присоединять их. В результате все эти ионы в той или иной концентрации будут содержаться в растворе. [13]
При помощи электронного микроскопа Мокрупшн, Китаев и Шабалина [36] изучали очень тонкие пленки гидроокиси меди, самопроизвольно образующиеся на поверхности водных растворов тетрааммиаката меди вследствие реакции гидролиза. Пленки состояли из коллоидных частиц, преимущественно размером 100 - 200 А, которые местами коагулировали с образованием двумерных или более толстых островков. Следовательно, здесь происходит поверхностная коагуляция коллоидных частиц гидроокиси меди, и в результате получаются однослойные или многослойные пленки из коллоидных частиц. Сходные результаты были получены также для пленок сульфида меди, образовавшихся на поверхности растворов сульфат меди после действия сероводорода [37]: пленки состояли из вторичных коллоидных частиц, образовавшихся при коагуля - - Ции первичных частиц сульфида меди и закрепленных, вследствие их гидрофобное, на поверхности раздела фаз раствор - газ. [14]
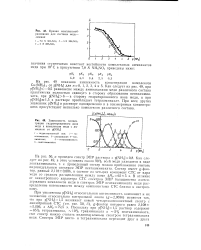 |
Кривая комплексооб-разования для системы медь -. шмиак.| Зависимость концентрации гидратированного иона меди и комплексов меди с аммиаком от pi [ NH3 ]. [15] |
Страницы: 1 2 3