Тетрааммиакат
Cтраница 2
Поскольку при p [ NH3 ] l 5 раствор содержит - 85 % тетрааммиака, - 10 % триаммиаката и - 5 % пентааммиаката, этот спектр можно считать индивидуальным спектром тетрааммиаката меди. [16]
Как следует из рис. 49, при р [ МНз ] - 0 5 равновесие между аммиакатами меди различного состава практически полностью сдвинуто в сторону образования пентааммиа-ката, при p [ NH3 ] 6 - в сторону гидратированного иона меди, а при p: [ NH3 ] l 5 в растворе преобладает тетрааммиакат. При всех других значениях p [ NH3 ] в растворе одновременно и в соизмеримых концентрациях присутствуют несколько комплексов различного состава. [17]
Тетрааммиакат сернокислой меди получается взаимодействием медного купороса CuSO4 - 5HaO с аммиаком. [18]
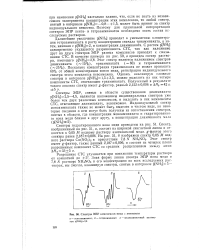 |
Спектры ЭПР комплексов меди с аммиаком. [19] |
МНз ] - 0 8 - hi 5, может быть принят за спектр индивидуального вещества. Поэтому для правильной интерпретации спектров ЭПР пента - и тетрааммиакатов необходимо знать состав исследуемых растворов. [20]
 |
Абсорбционная машина с твердым поглотителем. [21] |
Соединение СаС12 - 8МН3 соответствует максимальному насыщению. Соединение СаС12 - 8МН3 называется октааммиакатом, CaCls - 4NH3 - - тетрааммиакатом. [22]
Большинство важных в аналитическом отношении ионов металлов имеют несколько орбиталей, доступных для образования связей. Например, центральный ион меди может присоединять четыре молекулы аммиака с образованием плоского квадратного катиона - тетрааммиаката меди. [23]
Можно поступить и иначе: к раствору, содержащему катионы РЬ2 и Си2, сначала прибавить смесь винной кислоты с аммиаком и перевести простые катионы в разноименно заряженные комплексные ионы, а затем пропускать жидкость через Н - катионит. При этом комплексные анионы [ РЬ ( НС4Н4О6) з ] - будут переходить в фильтрат, а комплексные катионы тетрааммиаката меди - задерживаться катионитом. [24]
А затем пропускать жидкость через Н - катионит. При этом комплексные анионы [ РЬ ( НС4Н4Ов) 3 ] - будут проходить в фильтрат, а комплексные катионы тетрааммиаката меди - задерживаться катионитом. [25]
Ограничения толщины покрытий, полученных из водных сред, возникающие в результате появления внутренних напряжений, могут быть преодолены несколькими путями. Триплер, Бич и Фауст [9] добились улучшения защитных свойств платиновых покрытий из диамонодинитроплатиновых электролитов при использовании переменного тока, который также широко применяется для покрытий золотом. Высокопластичные пал-ладиевые покрытия толщиной до 5 мм были получены Стевенсом [12] из электролита бромид тетрааммиаката палладия. [26]
А затем пропускать жидкость через Н - катионит. При этом комплексные анионы [ РЬ ( НС4Н4О6) 3 ] - будут проходить в фильтрат, а комплексные катионы тетрааммиаката меди - задерживаться катионитом. [27]
Если реакция проводится в атмосфере водорода, а катализатором служит цеолит, не содержащий гидрирующего компонента - благородного металла, то на поверхности катализатора происходит отложение кокса, в результате чего каталитическая активность цеолита быстро снижается. Можно даже предположить, что роль благородного металла сводится только к подавлению коксообразования. Авторы работы [45] вводили платину и палладий в лантановую и аммонийную форму цеолита Y с SiO2 / Al2O3, равным 5 0, путем обмена в растворах, содержащих тетрааммиакаты платины и палладия, а затем изучали влияние содержания благородных металлов на активность. Оказалось, что даже небольшие количества благородных металлов повышают активность катализаторов изомеризации н-гексана. По мере увеличения содержания металла вплоть, до оптимального значения активность катализатора растет линейно. [28]
Поскольку ионный обмен цеолитов серии И осуществлялся из аммиачных растворов [1, 2], при прокаливании образцов на стадии их получения имеет место последовательный переход пентааммиакатов в тетра -, три - и диаммиакаты. После прогрева при 45 С на воздухе образцов CuNaY, адсорбировавших аммиак, наблюдается смещение максимума полосы поглощения до 16 500 см 1, что говорит о переходе по крайней мере части пентааммиакатов в тетрааммиакаты [32, 33, 37], поскольку низкочастотное плечо еще сохраняется. Повышение температуры до 75 С сопровождается смещением полосы до 15 700 см 1 и исчезновением низкочастотного плеча. [29]
Выделяющиеся молекулы аммиака адсорбируются цеолитом, что сопровождается появлением полос при 1415, 1460, 3340 и 3400 см 1, характерных для NH - HOHOB. В результате обработки при 350 С эти полосы из спектров удаляются и появляется сильная полоса при 3640 см-1. Если прогревание гидратирован-ного образца проводят в кислороде, платиновый комплекс сохраняет устойчивость вплоть до 200 С. Аммиак, выделяющийся при 250 С в результате разрушения тетрааммиаката платины, в этом случае цеолитом не адсорбируется. Возможно, что в присутствии кислорода разложение комплекса вызывается окислением NHa. Однако если перед восстановлением водородом окисленные образцы обработать водой, то часть платины может, выделиться в виде агрегатов, включающих несколько атомов платины. [30]
Страницы: 1 2 3