Тетрасиликат - калий
Cтраница 1
Тетрасиликат калия K2Si4O9 может быть получен сплавлением под давлением поташа с кремнеземом при температуре 500 - 600 и при нагревании калийного силикатного стекла с небольшим количеством воды. [1]
При температуре 592 С тетрасиликат калия испытывает знантаотропное превращение, поразительно похожее на а-нр-превраще-ние кварца. Общее сходство физико-химических свойств обоих кристаллических веществ, очевидно, обусловлено близким сходством их кристаллических структур. [2]
Результаты, полученные Мори и Феннером, дополняются фактом существования тетрасиликата калия, синтезированного Горансоном я Крачеком3 в гидротермальных условиях с небольшим количеством воды. [3]
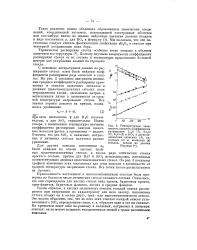
 |
Превращение KjSi4O9 на кривых. [4] |
Весьма интересные экспериментальные результаты были получены при изучении в этом направлении тетрасиликата калия KjO 4SiC2, плавящегося без разложения при нормальном давлении при 765 и образующего расплав, имеющий плотность, большую, чем кристаллическое вещество. При темпера-туре в 573 тетрасиликат ка-лия испытывает обратимое полиморфное превращение. [5]
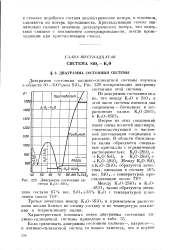 |
Диаграмма состояния системы К О-SiO.. [6] |
Третья эвтектика между K20 - 4Si02 и кремнеземом расположена весьма близко по своему составу и по температуре плавления к тетрасиликату калия. [7]
В этой системе быстро кристаллизуются только смеси, лежащие между мета - и дисиликатом калия, и смеси, содержащие более 90 % кремнезема; в области же образования тетрасиликата калия К2Э 4SiOj преобладает затвердевание в виде стекла. Это соединение кристаллизуется с таким трудом, что только с помощью гидротермальных методов можно получить центры его кристаллизации и использовать их в качестве затравок для кристаллизации переохлажденных расплавов. Кри стобалит и тридимит легко кристаллизуются из богатых кремнеземом стекол после предварительной выдержки их в гидротермальных условиях, согласно правилу Оствальда; то же относится и к кварцу, который кристаллизуется позже в виде хорошо развитых кристаллов. [8]
В проведенных нами исследованиях при испарении растворов силикатов калия ( 20 масс. % SiC2, 2 5 - 3 5) было обнаружено образование очень мало растворимых и практически не разлагающихся водой кристаллов гидрата тетрасиликата калия K. [9]
Неустойчивые равновесия между тетрасиликатом калия и эвтектиками кристобалита и тридимита были проверены специальными опытами. [10]
При давлении в 750 бар ( 1 бар соответствует давлению в 1 02 кг / см2) тетрасиликат становится уже ин-конгруэнтно плавящимся соединением, и на диаграмме состояния появляется реакционная точка К2О 4SiOa SSCh расплав. При увеличении давления до 1300 бар тетрасиликат калия вообще становится нестабильным в присутствии жидкой фазы, и в системе сохраняется только эвтектика между дисиликатом калия К О 2SliO2 и кварцем. [11]
Растворы силикатов калия при сушке требуют гораздо более осторожного обращения. Увеличение температуры до 90 - 100 G при сушке в массе или в пленке приводит к образований гидрата тетрасиликата калия K2O - 4SiO2 - H2O ( KHSi2O5), что идентифи-цируется рентгеноструктурным анализом. Количество KHSi2O5 в порошке, полученном при высокой температуре, может достигать половины общей массы. Технологические свойства жидкого стекла при этом в значительной степени утрачиваются. Низкотемпературная сушка в пленке т приводит к образованию видимых кристаллов KHSi2O5, жидкое стекло, содержащее 25 % SiO2, может слегка опалесцировать, щ порошок рентгеноаморфен. Распылительная сушка растворов силиката калия характерна малым временем процесса, что позволяет увеличивать температуру воздуха в зоне сушки без заметного образования плохорастворимого гидрата тетрасиликата калия. [12]
Исходя из теплоты плавления материала можно получить некоторые сведения о том, насколько внутренняя энергия неупорядоченной группировки атомов ( как в жидкости или стекле) превышает энергию правильной кристаллической решетки. Нитрат калия, не образующий стекла, имеет заметно меньшую теплоту плавления ( 25 кал-г 1), чем тетрасиликат калия ( 35 кал-г-1), являющийся наиболее устойчивым из двойных силикатных стекол. [13]
С помощью литературных данных по расширению стекол нами были найдены коэффициенты расширения ряда окислов в стекле. На рис. 2 показаны диаграммы изменения среднего коэффициента расширения кремнезема и окислов щелочных металлов в двойных щелочносиликатных стеклах поля тетрасиликата калия, дисиликата натрия и метасиликата лития в зависимости от средней температуры нагревания стекла. [15]
Страницы: 1 2