Тетрафенилборат - натрий
Cтраница 1
Тетрафенилборат натрия - удобный реагент для гравиметрического определения калия, так как калиевая соль состава К [ 1В ( С6Н5) 4 ] менее растворима, чем, например, хлористое серебро. Ион аммония мешает при этом определении и должен быть предварительно удален. Эта реакция не селективна, потому что данный реагент образует нерастворимые соли с ионами других одновалентных металлов, обладающих ( большими ионными радиусами, такими, как iAg ( I), T1 ( I), Cud), Gs ( I), Rb ( I), а также с некоторыми азотсодержащими органическими основаниями. [1]
Тетрафенилборат натрия, приблизительно 0 07 М раствор, 23 - 24 г тет-рафенилбората натрия растворяют в 500 мл дистиллированной воды в стакане емкостью 700 - 800 мл, добавляют 25 г гидроокиси или окиси алюминия и перемешивают стеклянной палочкой в течение 10 мин. Если первые порции фильтрата мутные, их собирают отдельно и вновь фильтруют. Осадок переносят из стакана на фильтр и промывают дистиллированной водой до тех пор, пока объем фильтрата не станет равным 950 - 980 мл. Титр раствора проверяют по хлориду калия через каждые 6 - 7 суток. [2]
Тетрафенилборат натрия в нейтральных и слабокислых растворах образует с ионом калия осадок тет-рафенилбората калия КВ ( С6Н5) 4 - Осаждение калия можно производить в кислых растворах ( рН около 1) в присутствии любых количеств натрия, магния и кальция. Осаждение калия может быть также выполнено в щелочной среде ( рН 8 - 9) в присутствии комплексона III, образующего с кальцием и магнием комплексы, не осаждающиеся тетрафенилборатом. [3]
Тетрафенилборат натрия является весьма ценным реактивом не только для открытия калия без предварительного удаления аммония, но и для количественного определения ряда веществ. [4]
Тетрафенилборат натрия Na B ( Сбн5) 4 - - очень важный ионный осадитель калия. Предложенный в 1951 г. Раффом и Броней41, этот реагент нашел широкое применение при решении многих аналитических проблем. В кислом растворе при рН 2 или при рН 6 5 в присутствии ЭДТА этот метод почти специфичен. Ртуть ( II), мешающая определению в кислом растворе, перестает оказывать мешающее действие при высоком значении рН в присутствии ЭДТА. Наиболее серьезное мешающее действие оказывают рубидий и цезий. [5]
Тетрафенилборат натрия Na B ( C6H5) 4 используют для осаждения иона калия. [6]
Раствор тетрафенилбората натрия, 3 % - ный, и промывная жидкость. Раствор оставтяют на ночь, затем к нему для коагуляции нерастворимого осадка добавляют 0 5 г гидроокиси алюминия. [7]
Тетранитрометан 527 Тетрафенилборат натрия 606 Тетра енилбораты 606 Teipai енилгексапентаен 296 Тетрш енилгидразин 569 Terpai енилметан 328 Тетра 1енилоктазен 595 Тетрафенилтетрацен ( Рубрен) 362 Тетра юнилциклотетрафосфин 59 Тетрафенилэтилен 342, 688 Тетрахлорэтан 413 Тетрахлорэтилен 413 Тетрацен 361 Тетрациклин 363 Тетраэтилпирофосфат 487 Тетраэтилсвинец 618 Тетраэтилсилан 605 Тетрит 447 и ел. [8]
При добавлении тетрафенилбората натрия к раствору соли таллия ( I) выделяется осадок. [9]
Подобно этому, тетрафенилбораты натрия, рубидия и цезия можно растворить в ацетоне. После разбавления раствора равным объемом воды в ионообменной колонке выделяется свободная кислота. [10]
При облучении раствора тетрафенилбората натрия в воде, освобожденной от воздуха, получают 97 % 1-фенилциклогекса-диена - 1 4 [37], который на воздухе превращается в бифенил. Сдваивание колец идет внутримолекулярно, а связь между ними осуществляется за счет углеродных атомов, первоначально связанных с бором. [11]
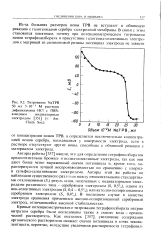 |
Титрование NaTPB 50 мл 5 - 10 - 3 М раствора дифениламина НС1 с ПВХ-амидным индикаторным электродом ( ( г Am. Chem. Soc.. [12] |
Кривые потенциометрического титрования тетрафенилбората натрия нитратом серебра были исследованы также в смесях вода - органический растворитель. [13]
Осаждение ионов калия тетрафенилборатом натрия является одним из первых примеров обратного титрования с использованием осадителя. Растворимость тетрафенилбората натрия в воде недостаточна для получения растворов такой концентрации, которая обычно требуется для термометрического титранта. Поэтому известное и избыточное количество тетрафенилбората натрия прибавляют к раствору пробы, содержащему ионы калия. Смесь перемешивают и выдерживают несколько минут до наступления термического равновесия. Затем избыток фенилбората титруют концентрированным раствором хлорида калия. [14]
Ценными аналитическими свойствами обладает тетрафенилборат натрия NaB ( C6Hs) 4, осаждающий ионы калия, аммония и некоторые другие. Можно назвать также купферон, антраниловую кислоту, арсеновые кислоты, диантипирилметан и многие другие органические реагенты, эффективно используемые в гравиметрическом анализе. [15]
Страницы: 1 2 3 4