Тетрафторборат
Cтраница 2
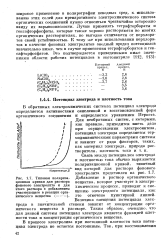 |
Типовая поляриза - Добавление в раствор органического. [16] |
Лучше применять тетрафторбораты и гексафторфосфаты, которые также хорошо растворяются во многих органических растворителях, но выгодно отличаются от перхлоратов своей устойчивостью. К тому же при использовании перхлорат тов в качестве фоновых электролитов анодный предел потенциалов значительно ниже, чем в случае применения тетрафторборатов и гек-сафторфосфатов. [17]
Электроотрицательный ион тетрафторбората [ BF41 - образует с ионом тетрафениларсония [ ( CeH5) 4As ] ионную пару, экстрагируемую хлороформом. Замена иона тетрафениларсония положительно заряженными ионами красителей позволяет одновременно отделять и определять бор фотометриче скнм методом. [18]
Для определения тетрафторбората применены ионоселективные электроды. Один из методов основан на титровании BFI раствором ТФАХ при 2 С. Конец титрования устанавливают ионоселек-тивным электродом ( Орион) с жидким ионообменником, чувствительным к ионам СЮ4 и BFJ. Определению мешают нитраты и иодиды. [19]
Термическое разложение тетрафторборатов диазония по Шиману [884, 909] служит одним из методов ведения атома фтора в ароматическое кольцо. Тетрафторбораты диазония, отличающиеся ограниченной растворимостью в воде и высокой стабильностью, получают добавлением тетрафторборной кислоты и ее солей при или после диазотирования амина в минимальном количестве воды. Осадок тетрафторбората отделяют, промывают и тщательно высушивают. [20]
При реакции тетрафторборатов диазония с ацетатом палладия под давлением СО в ацетонитриле в присутствии ацетата натрия образуются карбоновые кислоты ( см. разд. [21]
При нитровании тетрафторборатом нитрония было выделено 85 2 % 4-из. Однако при нитровании 4-изопропилтолуола ( 47) ацетилнитрйтом наряду с примерно теми же количествами 3-нитропроизводного ( 54) и 4-нитротолуола ( 55) выделены 41 % 2-нитропроизводного ( 53) а также 41 % циклогексадиена ( 52), который легко превращается в 2-нитроизомер ( 53) в серной кислоте. [22]
Гораздо удобнее получать устойчивые тетрафторбораты диазо-ния, которые выпадают в виде труднорастворимых солей при дй-азотировании в 40 % - ной тетрафторбороводородной кислоте. [23]
Гравиметрический метод определения тетрафторбората осаждением его нитроном в виде C2oHi6N4HBF4 имеет ряд недостатков. Один из них связан с высокой растворимостью осадка, вследствие чего при расчете используют эмпирический коэффициент. [24]
В некаталитической реакции тетрафторбората арилдиазония с иодидом калия в метаноле при О С было обнаружено образование арилиодида наряду с продуктами окислительно-восстановительных процессов, такими, как арены и формальдегид. [25]
С диазометаном или тетрафторборатом триметялоксония, характерным реагентом на подвижные водородные атомы, и в частности на водородный атом гидроксильной группы, ацетоуксусный эфир образует метиловый эфир g - оксикротоновой кислоты: таким образом были выделены устойчивые производные кетонной и енольной форм ацетоуксусного эфира. [26]
По-видимому, особенно агрессивен тетрафторборат фтордиазония. Гексафторантимонат энергично реагирует с нитрометаном, нитробензолом, четыреххлори-стым углеродом, фреонами, двуокисью серы ( образуются SOF2, SOaF2, SOa - SbF5, N2O, N2), в жидком фтористом водороде нерастворим или растворим весьма плохо. Растворитель для него подобрать не удалось, поскольку со всеми веществами он реагирует. [27]
Эфирные фильтраты после отделения тетрафторбората 2 6-дифенилтиопирилия объединяют, промывают водой до нейтральной реакции, сушат прокаленным Na2SO4 - Эфир отгоняют, остаток кристаллизуется. [28]
Описан спектрофотометрическии метод определения тетрафторбората с помощью ферроина [5], основанный на избирательной экстракции ионного ассоциата н-бутиронитрилом и измерении поглощения при 520 нм. При однократной экстракции извлекается 74 % тетрафторбората. Закон Бера соблюдается в широком интервале концентраций. [29]
Реакцию проводят термическим разложением твердого тетрафторбората арендиазония. [30]
Страницы: 1 2 3 4