Тетрафторборат - натрий
Cтраница 1
Тетрафторборат натрия [172] также реагирует с гидридом натрия с образованием боргидрида. Удобно проводить эту реакцию, обрабатывая NaBF4 ( можш в масляной суспензии) водородом при атмосферном или повышенном давлении в присутствии металлического натрия при 250 - 280 С. Ниже 250 С реакция идет слишком медленно, а выше 280 С начинают идти побочные реакции, что приводит к падению выхода. [1]
Стандартные растворы готовят, растворяя точную навеску тетрафторбората натрия. Концентрацию тетрафторборат-ионов в электролите либо определяют непосредственно, используя микропроцессорный ионономер lonalyzer ( модель 901), либо рассчитывают по калибровочному графику. [2]
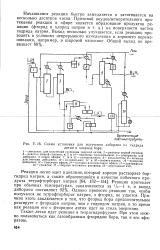 |
Схема установки для получения диборана из гидрида лития и хлорида бора. [3] |
Однако провести реакцию так, чтобы получался не тетрафторборат натрия, а фторид, не удается. Причина этого заключается в том, что фторид бора предпочтительнее реагирует с фторидом натрия, чем с гидридом натрия, в то время как реакция его с фторидом лития идет не столь энергично. [4]
Характерно, что при взаимодействии алюмогидрида натрия с тетрафторборатом натрия в диглиме при 80 - 90 С получается не диборан, а только боргидрид натрия. Для получения диборана при 80 - 100 С на 3 моль NaAlH4 фактически расходуется 4 4 - 4 8 моль BF3 вместо 4 моль по теории. [5]
Перед работой индикаторный электрод выдерживают в 0 1 М растворе тетрафторбората натрия, этот же раствор используют для хранения электрода. Перед измерениями электрод промывают несколько раз дистиллированной водой и обсушивают фильтровальной бумагой, добиваясь стабильного потенциала фонового электролита. [6]
 |
Электролизер для электросинтеза органических соединений.| Электролизер для электроорганического синтеза с псевдосжиженными электродами. [7] |
Потенциал разряда, применяемого при электролизе тетрафторбората BFT, еще более положителен, чем у перхлората. Тетрафторборат натрия NaBF4 растворим во многих органических веществах. [8]
 |
Схема прибора для получения. [9] |
Для приготовления тетрафторбората натрия к 25 г плавиковой кислоты ( 40 % - ный раствор), находящейся в охлаждаемой льдом платиновой чашке, прибавляют небольшими порциями 6 2 г борной кислоты и смесь оставляют стоять в течение 6 ч при комнатной температуре. Затем снова помещают чашку в баню со льдом, охлаждают и ней - трализуют содержимое, добавляя 5 3 г безводного бикарбоната натрия. Раствор упаривают до начала кристаллизации и - после охлаждения отделяют выделившиеся кристаллы, которые затем высушивают в вакууме. [10]
 |
Схема прибора для получения трехфтористого бора. [11] |
Для приготовления тетрафторбората натрия к 25 г плавиковой кислоты ( 40 % - ный раствор), находящейся в охлаждаемой льдом платиновой чашке, прибавляют небольшими порциями 6 2 г борной кислоты и смесь оставляют стоять в течеиие 6 ч при комнатной температуре. Затем снова помещают чашку в баню со льдом, охлаждают и ней - трализуют содержимое, добавляя 5 3 г безводного бикарбоната натрия. Раствор упаривают до начала кристаллизации и - после охлаждения отделяют выделившиеся кристаллы, которые затем высушивают в вакууме. [12]
Тетрафторборатный электрод заряжают в соответствии с инструкцией, изложенной в паспорте. Собранный электрод выдерживают при комнатной температуре в течение суток в 0 1 М растворе тетрафторбората натрия. [13]
При добавке алюмогидрида натрия к раствору фторида бора в диглиме на холоду диборан выделяется сразу. Увеличение количества подаваемого алюмогидрида не вызывает повышения выхода, однако если добавить алюмогидрид и нагреть до 100 С, то образовавшийся тетрафторборат натрия вступает в реакцию. [14]
Это связано с тем, что продукт реакции - хлорид натрия нерастворим в диглиме, в то время как продукт реакции с фторидом бора - тетрафторборат натрия немного растворим. [15]
Страницы: 1 2