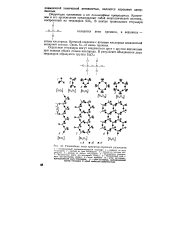
Отдельный тетраэдр
Cтраница 1
Отдельные тетраэдры могут соединяться друг с другом вершинами при помощи общих атомов кислорода. [2]
Они построены из отдельных тетраэдров SiO4, связанных с металлами, как в оливине ( рис. 3.4 6) или гранате. Эти минералы имеют четыре атома кислорода, не входящих в мостики, и известны также как орто-сюшкаты. [3]
Образование структур с отдельными тетраэдрами [ Si64 ] ( с единичным островным расположением) и полимеризация более сложных форм, цепочек, дву - и трехмерных сеток тесно связаны с физико-химическими условиями самого процесса кристаллизации. Совершенно очевидно, что в процессе дифференциации магматических расплавов6 ранние кристаллические выделения обогащены силикатами с единичными тетраэдрами [ Si04 ], образующими в структуре острова, - оливинами. При понижении1 температуры, из-за избытка катионов в расплаве, число имеющихся анионов кислорода оказывается недостаточным для насыщения всех катионов. В результате несколько тетраэдров объединяются в структурную единицу при помощи образующихся кислородных мостиков. Таким образом, при понижении температуры развиваются цепочечные структуры пироксенов или амфиболов, а также образуются двумерные сетки слюд и - родственных им минералов. Наконец, возникают каркасы кремнезема и при участии ионов А13 - каркасы типичных алюмосиликатов. Вполне возможно, что при быстром падении температуры в этих трехмерных аранжировках скорость атомных перераспределений становится слишком малой для образования правильной кристаллической формы. Так именно и образуются неполностью упорядоченные каркасы, характерные для структур переохлажденных стекол Их переходом в твердое состояние заканчивается магматический; процесс образования горных пород из расплавов. [4]
Если справедлив такой механизм образования пар, то отдельные тетраэдры должны быть ориентированы определенным образом. Такой же механизм возможен и при образовании тройных тетраэдров, хотя их образование менее вероятно, чем образование пар. [5]
Кристалл кварца - гигантская молекула, состоящая из отдельных тетраэдров SiO4, в которых каждый атом кремния окружен четырьмя атомами кислорода, а каждый атом кислорода является общим угловым атомом для двух таких тетраэдров. [6]
Кроме этих трех бесконечных серий, в таблице приведены несколько отдельных тетраэдров, равно-составленных с кубом. [7]
Для тетраэдрических полостей в шапочных дельтаэдрах необходимо локализованное связывание, как в случае отдельных тетраэдров. Тетраэдрические полости, образованные введением шапок в дельтаэдры со всеми вершинами степени больше 3, могут рассматриваться как острова локализации связывания в системе, делока-лизованной в остальной части. [8]
Структурной единицей, характерной для всех фосфатов, является тетраэдр РО4, в котором атом фосфора тетраэдрически окружен четырьмя атомами кислорода. Отдельные тетраэдры связаны общими атомами кислорода. [9]
 |
Удельная проводимость у и. [10] |
Асбест представляет собой минерал, обладающий волокнистым строением. Связь между отдельными тетраэдрами в кольце и между соседними звеньями осуществляется через общие ионы кислорода. Волокна асбеста напоминают по своим свойствам растительные волокна, но имеют значительно большую толщину и отличаются большей гигроскопичностью. Асбест обладает стойкостью к действию щелочей, но реагирует с кислотами. В состав асбеста входит химически связанная вода, выделение которой начинается примерно при 400 С. Это сопровождается распадом волокна асбеста и резким снижением его механической прочности; поэтому предельно допустимой температурой считают 350 С. Плавление асбеста начинается при 1150 С. Наличие примесей, в частности, окислов железа обусловливает высокую проводимость 7 1 ( Г9 1 / ом-см, даже сухого, но непропитанного асбеста. Из асбестового волокна нередко с добавлением целлюлозного или синтетического волокна изготовляют пряжу, ленту, ткань и картон. Асбест применяют также как наполнитель в пластмассах. [11]
 |
Решетка оливина ( Mg, Fe2 [ Si 04 ]. [12] |
Если на каждый ион Si4 стехиометрически приходится меньше четырех ионов О2, то этот принцип построения сохраняется благодаря тому, что ионы 02 - могут быть общими для соседних тетраэдров. Между отрицательными комплексными ионами, состоящими из отдельных тетраэдров SiO или из тетраэдров, соединенных между собой общими ионами О2, расположены положительные ионы, участвующие в построении кристалла. Эти ионы располагаются возможно дальше друг от друга, и, как вообще в координационных решетках, группируют вокруг себя как можно ближе и больше отрицательных ионов ( в данном случае ионов О2 тетраэдров SiC) 4) ( ср. На основании внутреннего строения силикаты подразделяют на соединения с островными структурами, с цепочечными и ленточными структурами, со слоистыми и с пространственными сетчатыми структурами. [13]
Диоксид кремния SiO2 ( кремнезем) имеет несколько модификаций, из которых наиболее распространен кварц. Кристалл кварца представляет собой гигантскую полимерную молекулу, состоящую из отдельных тетраэдров, в которых каждый атом Si окружен четырьмя атомами кислорода, а каждый атом кислорода осуществляет мостиковую трехцентровую связь, являясь общим угловым атомом для двух тетраэдров. [14]
 |
Зависимость энергии. [15] |
Страницы: 1 2