Толщина - слой - электролит
Cтраница 3
Для того чтобы установить причины столь сильного облегчения скорости катодной реакции восстановления кислорода по мере уменьшения толщины слоя электролита, необходимо рассмотреть - механизм переноса кислорода через тонкие слои электролита. [31]
Из уравнения ( 5 2) следует, что скорость движения растет с величиной градиента температуры и толщиной слоя электролита. Последний вывод справедлив лишь для тон. [32]
Коррозия в морской атмосфере отличается от коррозии в морской воде в основном тем, что она связана с малой толщиной слоя электролита на поверхности корродирующего металла. Скорость морской атмосферной коррозии зависит от влажности воздуха, количества осадков, температуры, различных загрязнений и агрегатного состояния воды. При относительной влажности воздуха около 100 %, а также при непосредственном попадании влаги на металл коррозия металлов относится к типу мокрой атмосферной коррозии. [33]
Установлено, что катодный процесс ионизации кислорода на железе, меде, никеле и цинке облегчаете по мере уменьшения толщины слоя электролита на поверхности металла. [34]
 |
Задание проницаемых завес. [35] |
ДМз - длина завесы ( по ее фронту), приходящаяся на данное сопротивление; рэ - удельное сопротивление и 6Э - толщина слоя электролита в данном месте. [36]
 |
Влияние толщины пленки электролита на анодную поляризацию меди в 0 01 N растворе NaCl. [37] |
Кривые анодной поляризации меди, полученные в 0 01 N растворе NaCl ( рис. 76) показывают, что анодный процесс при уменьшении толщины слоя электролита замедляется в несколько раз. Так, например, при толщине пленки 70 мк в 0 01 JV растворе NaCl потенциал анода становится уже при плотности тока в 200 мка / см2 равным 1 в. Как будет показано ниже, это в значительной степени связано с пассивирующим действием окисных пленок, возникающих при электрохимическом окислении меди в тонких слоях гораздо легче, чем в объеме. Этому явлению в значительной степени способствуют нерастворимые продукты анодной реакции, осаждающиеся на поверхности электрода. [38]
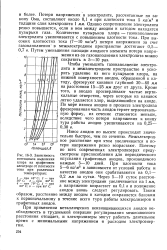 |
Зависимость потенциала выделения хлора на графитовом электроде от плотности тока при различных температурах. [39] |
Потери напряжения в электролите, рассчитанные по закону Ома, составляют около 0 1 в при плотности тока 5 ка / м2 и толщине слоя электролита 1 мм. Однако сопротивление электролита резко повышается, если в нем между анодом и катодом находятся пузырьки газа. Количество пузырьков хлора - газонаполнение электролита увеличивается с повышением плотности тока. При высоких плотностях тока ( 7 - 10 ка / м2) потери напряжения за счет газонаполнения1 в межэлектродном пространстве достигают 0 5 - 0 7 в. [40]
 |
Схема двухэлектродной системы, иллюстрирующая принцип расчета распределения тока. [41] |
Однако, сделав допущение, что имеется линейная зависимость потенциала от плотности тока ( как будет показано ниже, это оправдано) и учитывая, что толщина слоя электролита меньше протяженности / электродов, можно вывести уравнения, которые позволяют рассчитать плотность тока на любом расстоянии от границы контакта двух разнородных металлов. [42]
Если известны законы изменения толщины слоя в процессе испарения, а также зависимость скорости кислородной деполяризации от толщины пленки, можно определить, увеличивается ли эффективность работы катодов благодаря изменению толщины слоя электролита или имеют место другие явления. [44]
В условиях диффузионного режима эффективность работы катода ( плотность тока на нем), начиная с определенной величины ( 0 05 - 0 07 см), должна возрастать по мере уменьшения толщины слоя электролита по законам, свойственным диффузионным процессам. Расчеты и опыты, которые будут описаны ниже, показывают, однако, что, когда мы имеем дело с тонкими слоями, явление сильно осложняется. Диффузионные токи, регистрируемые экспериментально, значительно выше тех значений, которые получаются путем расчета при допущении, что в слоях тоньше 0 05 - 0 07 см кислород переносится по чисто диффузионному механизму. [45]
Страницы: 1 2 3 4 5
