Трис-буфер
Cтраница 2
 |
Схематическое изображение - я, с одной стороны, к сбли-тройного комплекса цинк-трис-пени - жению реагентов ( пеницил-циллии. лина и трис-буфера, а с. [16] |
Отсутствие реакционной способности у ионов Си2 и Ni2 вплоть до концентраций 10 3 моль / л и рН 8, вероятно, результат хелатирования ионов металлов трис-буфером, затрудняющего взаимодействие с пенициллином. [17]
Пластинки, выделенные, как указывалось выше, взвешивали в изотоническом ( 0 25 М) растворе сахарозы с добавлением 0 1 М ЭДТА или в 0 05 М трис-буфере с добавлением ЭДТА. [18]
Реактивы и оборудование: 1) 0 5 % - ный раствор гипохлорита натрия, 2) жидкий азот, 3) 0 15 М NaCl - 0 01 М ЭДТА - 0 05 М трис-буфер, рН 8 2, 4) 5 % - ный спиртовой раствор ДДС, 5) 5 М NaClO4, 6) хлороформ - изоами-ловый спирт ( 24: 1), 7) 96 % - ный этанол, 8) 10XSSC, 9) 0 1XSSC, 10) ри-бонуклеаза, 11) 3 М ацетат натрия - 0 01 М ЭДТА, рН 7 0, 12) изопропанол, 13) хлороформ, 14) центрифуга с охлаждением, 15) термостат, 16) блендор, 17) механическая мешалка, 18) фарфоровая ступка, 19) мерные цилиндры от 0 025 до 1 л, 20) колбы Эрлеямейера от 0 1 до 3 л, 21) пипетки, 22) шприц стеклянный на 50 - 100 мл для отсасывания слоев. [19]
В гелях, которые содержат активные сложно-эфирные группы для прямого ковалентного связывания ( например, активированная СН-сефароза, аффигель 10 или оксиалкилметакрилатные гели с я-нитрофенильной сложно-эфирной группой), непрореагировавшие группы удаляют путем обработки 0 1 М трис-буфером ( рН8): через 1 ч в геле практически не остается групп, способных связывать белки или пептиды. Для носителей, которые содержат альдегидные группы в качестве активных связывающих групп, после связывания преимущественно используется восстановление борогид-ридом натрия. При этом происходит и восстановление остающихся альдегидных групп, стабилизация связей между белком и нерастворимой матрицей. [20]
В опытах 1 мл 0 2 % - ного по железу насыщенного ферритина был подвергнут диализу против 10 мл 0 2 % - ного Рз-трансферрина, 1 0 мМ аскорбиновой кислоты, 1 0 мМ АМФ в 0 1 М трис-буфере, рН 7 4 [ воспроизводится с разрешения Дж. [21]
Наряду с 0 02 - 0 05 М фосфатным буфером рН 6 7 - 6 8 для забуферивания растворов NaCl используют 0 025 М трис-буфер рН 7 0 [18], 0 01 М трис - HCl буфер рН 8 5 [42], 0 02 М трис - НС1 буфер рН 7 4 [13] и др. Обычно трис-буфер применяют при хроматографии тотальных препаратов НК для лучшего отделения РНК от ДНК. [22]
Для приготовления 0 5 мл раствора ДНК - количества, достаточного для заполнения ячейки с 12-миллиметровым двухградусным сектором, - смешивают 0 2 мл насыщенного раствора CS2S04 ( при 23 - 24), 0 25 - 0 5 мкг ДНК ( в расчете на одну полосу) и 0 3 мл воды или 0 001 М трис-буфера. Конечную плотность раствора подбирают таким образом, чтобы полоса ДНК располагалась примерно в центре ячейки. Для приготовления образцов РНК насыщенный раствор CS2S04 смешивают с раствором 0 5 - 1 мкг РНК в 0 1 М фосфат-цитратном буфере, к раствору затем обычно добавляют формальдегид, до концентрации 1 - 2 %, чтобы предотвратить агрегацию и осаждение высокомолекулярной РНК [8] ( см. разд. Приготовление образцов в смеси растворов Cs2S04 и CsCl описано в разд. Для приготовления раствора неизвестного образца ДНК в CsCl смешивают 0 4 мл насыщенного раствора CsCl и 0 5 - 1 мкг ДНК в 0 1 мл воды или т рис-буфера. Чтобы гидростатическое давление во всех случаях было одинаковым, ячейки необходимо заполнять до одного и того же уровня так, чтобы высота воздушного столба составляла около 5 % высоты ячейки. [23]
Гюильбо и др. [663] исследовали катион-селективные стеклянные электроды Бекман 39047 и 39137 для определения уреазы, глутами-назы, аспарагиназы и оксидаз о - и L-аминокислот. К известному объему трис-буфера ( рН 7 0) добавляют определенный объем анализируемого раствора фермента. Индикаторный электрод и электрод сравнения ( нас.к.э.) погружают в раствор, после чего потенциал записывается автоматически. Потенциал, соответствующий наименьшей концентрации NH. Большой положительный потенциал указывает на присутствие катионов щелочных металлов, которые воздействуют на электродную функцию. Потенциал меняется как функция концентрации образовавшихся ионов аммония. Количество имеющегося фермента можно рассчитать из кривой зависимости ДЕ / мин от концентрации фермента. [24]
Ей отвечало динамическое равновесие, при котором незначительная часть молекул Трис находилась в растворе в виде ионов Трис, а подавляющее большинство их было незаряжено. При его добавлении происходит как бы титрование Трис-буфера кислотой. Первоначальное равновесие нарушается: теперь большее число молекул Трис приобретает положительный заряд, однако несколько увеличивается и равновесная концентрация протонов в растворе - он понемногу ( буферный эффект. Этому моменту отвечает превращение почти всех молекул Трис в положительные ионы, так как буферная емкость Трис-буфера при таком рН уже практически исчерпывается. [25]
Эта часть эксперимента очевидна - из крепкого раствора СА белки высаливались и переходили на гидрофобную матрицу. Далее осуществлялась ступенчатая элюция - сначала просто 0 01 М трис-буфером; заметная доля белков при этом выходила из колонки, но далеко ие все. [26]
Более крупные, чем микоплазма, клетки содержат различные специализированные структуры, к числу которых относятся митохондрии, микросомы, пластиды ( в растительных клетках), лизосомы и др. Они могут быть выделены из гомо-генатов клеток различных растительных и животных тканей. Для этой цели ткани измельчаются и гомогенизируются в гипертоническом фосфатном или трис-буфере с добавлением сахарозы при температуре 0 - 4 С, а затем проводится дифференциальное центрифугирование гомогенатов. В качестве примера приводим схему центрифугирований для получения отдельных субклеточных и пластидных фракций растительной клетки. [27]
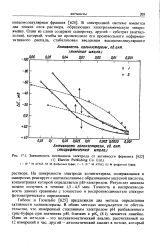 |
Зависимость потенциала электрода от активности фермента ( Elsevier Publishing Co. Ltd.. [28] |
Гибсон и Гюильбо [625] предложили два метода определения активности холинэстеразы. В обоих методах используется то обстоятельство, что измеренный стеклянным электродом рН разбавленного трис-буфера при значениях рН, близких к рКа (8.1), меняется линейно. [29]
Процедура определения заключалась в следующем: 1 мл раствора аргиназы впрыскивали в буферный раствор ( 0 1 М трис-буфер, рН 7 5), содержащий аргинин, и следили за изменением во времени потенциала уреазного электрода, включенного против НКЭ. [30]
Страницы: 1 2 3