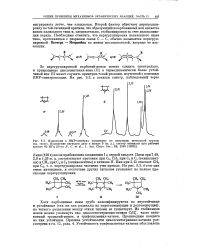
Трифенилметил-катион
Cтраница 2
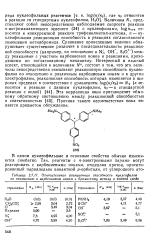 |
Относительная реакционная способность нуклеофилов по отношению к карбениевым ионам и бромистому метилу в водной среде. [16] |
Величины N представляют собой непосредственно наблюдаемые скорости реакции n - нитромалахитового зеленого ( 24) с нуклеофилами, logKOTH относится к конкурентной реакции трифенилметил-катиона, п - ну-клеофильная реакционная способность в реакциях согласованного замещения метилбромида. Сравнение приведенных величин обнаруживает существенное различие в последовательности реакционной способности ( например, по отношению к Ыз, ОН, S2O, ) между реакциями с участием карбениевых ионов и реакциями, проходящими по согласованному механизму. Причина такого несоответствия пока является предметом обсуждения. [17]
Предпочтительность планарного расположения для сопряженных карбониевых ионов очень наглядно подтверждается в точных кристаллографических исследованиях трифеншщиклопропенил-катиона (5.12) [1250], в котором фенильные кольца находятся несколько дальше друг от друга, чем в трифенилметил-катионе. В результате этого система может ближе подойти к планарному расположению. Углы поворота колец составляют 7 6; 12 1 и 21 2, причем их неравенство относят за счет различия в упаковке фенильных групп в твердом веществе. [18]
Первый интенсивно изучавшийся класс карбоний-ионов - трифенилметил-катионы и близкие им ионы. Известно очень большое число трифенилметил-катионов с заместителями в ароматическом кольце, многие из них в виде кристаллических солей. [19]
Другой иллюстрацией может служить такая классическая защита спиртов, как тритпльная. Оказывается, что и довольно специфических условиях - при катализе реакции трифенилметил-катионом - она превращается в функциональную группу и подвергается диспропорцио-нировашпо. [20]
Хотя карбониевые ионы грубо классифицируются на неустойчивые и устойчивые ( так же как радикалы на короткоживущие и долгоживущие), но четкого разделения между этими типами не существует. Из стабильных ионов можно упомянуть два: циклогептатриенил-катион С7Щ, часто называемый тропилий-ионом, и трифенилметил-катион. [22]
Вклады нескольких поляризуемых групп в делокализцию заряда суммируются. Поэтому, например, исключительно высокой стабильностью обладают триарилметильные коны. Так, и борфторид трифенилметил-катиона ( 35), и трифенилметилнатрий ( 36) имеют чисто ионную структуру - случай, достаточно редкий для соединений, несущих заряд на атомах углерода. [23]
Вклады нескольких поляризуемых групп в делокализцию заряда суммируются. Поэтому, например, исключительно высокой стабильностью обладают триарилметильные ионы. Так, и борфторид трифенилметил-катиона ( 35), и трифенилметилнатрий ( 36) имеют чисто ионную структуру - случай, достаточно редкий для соединений, несущих заряд на атомах углерода. [24]
Согласно данным, полученным; при исследовании оптических спектров таких очень стабильных катионов, как трифенилметил-катион, плоский тригональный карбониевый ион удерживается на поверхности в основном электростатическими силами. Правда, этот катион имеет довольно большие размеры и еще более крупным из-за тетраэдрической конфигурации молекулы является его предшественник. Поэтому в действительности трудно сказать, находится ли трифенилметил-катион в порах цеолита или только на внешней поверхности. Другой крайний случай представляет собой присутствие на поверхности катализатора протона, который образует ковалентную связь с отдельным атомом кислорода каркаса. Кислотность такого центра проявляется в его способности отщепить протон и протонировать находящиеся поблизости молекулы какого-либо основания. Ковалентная и ионная связи катиона с каркасом изображены на схемах 22 и 23 соответственно. Какая же из этих схем лучше отражает взаимодействие в / ио - бутил-катиона с поверхностью. [25]
Первый общий метод, основанный на относительной реакционной способности различных карбониевых ионов, редко представляет практический интерес, поскольку, если ион карбония настолько устойчив, что может присутствовать в растворе в аналитически определяемых количествах ( как это требуется в кинетических опытах), то проще применить в этом случае метод равновесия. Поэтому эксперименты в этом направлении представляют интерес главным образом в связи с другими данными. Сравнение скоростей отрыва гидрид-иона трифенилметил-кати-оном и его 4 4 4 -триметоксианалогом [56], при котором было найдено, что последний ион примерно в 1000 раз менее реак-ционноспособен, чем трифенилметил-катион, подтверждает данные по их относительной стабильности, полученные при изучении равновесий. С другой стороны, ди - ( 4-метоксифенил метил-катионы реагируют немного быстрее, чем трифенилметил-катионы, хотя индикаторные измерения на соответствующих спиртах указывают на большую стабильность первого из этих ионов. [26]
Одной из наиболее обычных реакций карбениевых ионов, широко представленной в процессах 5 1, является взаимодействие с неподеленной ( п) парой электронов нуклеофила. В качестве ну-клеофилов могут выступать анионы, например R0 -, СГ, N3, или нейтральные молекулы ( например, ROH, СО); в последнем случае устойчивые, электрически нейтральные молекулы могут образоваться только за счет последующей реакции, такой как перенос протона. Эти реакции проходят обычно очень быстро, и их скорости могут быть надежно измерены только в случае очень устойчивых карбениевых ионов типа триарилметила. Однако бензил -, ди-фенилметил - и трифенилметил-катионы, генерированные импульсным радиолизным методом в дихлорэтане [43], реагируют с гало-генид-ионами с диффузно-контролируемыми скоростями. Чаще всего для оценки реакционной способности нуклеофилов используют метод конкурентных реакций. [27]
Первый общий метод, основанный на относительной реакционной способности различных карбониевых ионов, редко представляет практический интерес, поскольку, если ион карбония настолько устойчив, что может присутствовать в растворе в аналитически определяемых количествах ( как это требуется в кинетических опытах), то проще применить в этом случае метод равновесия. Поэтому эксперименты в этом направлении представляют интерес главным образом в связи с другими данными. Сравнение скоростей отрыва гидрид-иона трифенилметил-кати-оном и его 4 4 4 -триметоксианалогом [56], при котором было найдено, что последний ион примерно в 1000 раз менее реак-ционноспособен, чем трифенилметил-катион, подтверждает данные по их относительной стабильности, полученные при изучении равновесий. С другой стороны, ди - ( 4-метоксифенил метил-катионы реагируют немного быстрее, чем трифенилметил-катионы, хотя индикаторные измерения на соответствующих спиртах указывают на большую стабильность первого из этих ионов. [28]
Одно-электроиное кулонометрическое окисление при потенциале первой вольтамперометрической волны в смеси трифторуксусная кислота - дихлорметан дает раствор, содержащий катион-радикал ДФА. Последующее ( дополнительное) одноэлектронное кулонометрическое окисление при потенциале, отвечающем образованию дикатиона, приводит к практически полному расходованию катион-радикала. В результате двухэлектронного кулонометрического восстановления полученного раствора полностью регенерируется ДФА. Видимый спектр карбениевого иона 9, приготовленного двухэлектронным окислением ДФА в присутствии трифторуксусной кислоты, имеет максимум поглощения при 416 нм, что можно рравнить со значением 441 нм для трифенилметил-катиона. [29]
Страницы: 1 2