Изолейцин
Cтраница 2
Взаимодействие изолейцина с регуляторным центром треониндегидратазы не сопровождается образованием ковалентных связей и потому легко обратимо. Треониндегидра -, таза-типичный представитель класса аллостерических, или регуляторнъгх, ферментов, которые осуществляют свои функции путем обратимого нековалент-ного связывания с молекулой, модулятора. [16]
Образование изолейцина, валина и лейцина. [17]
Лейцин и изолейцин под влиянием некоторых микроорганизмов, например дрожжей, превращаются в спирты, молекулы которых содержат на один атом углерода меньше, чем молекулы взятых аминокислот. При этом от молекулы аминокислоты отщепляется СО2, а аминогруппа замещается гидроксилом. [18]
Лейцин и изолейцин не только входят в состав белков, но часто содержатся в растениях в большом количестве и в свободном состоянии. Они могут быть источниками сивушных масел при спиртовом брожении. Валин, лейцин и изолейцин по своим свойствам близки один другому, и их разделение обычными химическими методами достигается с трудом, а лейцин и изолейцин трудно разделить даже при использовании хрома-тографических методов анализа. [19]
Лейцин и изолейцин являются важными аминокислотами, входящими в состав белков. Норлейцин ( а-амино-н-капроновая кислота) приготовлен синтетически и в белках не найден. [20]
Лейцин и изолейцин под влиянием некоторых микроорганизмов, например дрожжей, превращаются в спирты, молекулы которых содержат на один атом углерода меньше, чем молекулы взятых аминокислот. При этом от молекулы аминокислоты отщепляется СО2, а аминогруппа замещается гидроксилом. [21]
Лейцин, изолейцин и валин легко образуют смешанные кристаллы и трудно отделяются друг от друга. [22]
Лейцин и изолейцин на многих силиконах не разделяются. [23]
Лейцин, изолейцин, метионин и цистин. [24]
Лейцин и изолейцин образуются из белковых веществ такжй при гидролизе в присутствии щелочи или кислоты. [25]
Лейцин и изолейцин - оптически деятельны. Аминокислоты пот влиянием дрожжей ( содержащихся в них ферментов) превращаются в спирты, содержащие на один углеродный атом меньше, чем взятая кислота: отщепляется углекислый газ, а аминогруппа замещается гидроксилом. [26]
Лейцин и изолейцин представляют собой изомеры а-аминоизо-капроновой кислоты, образуются при гидролизе белков и, следовательно, принимают участие в образовании белковой молекулы. [27]
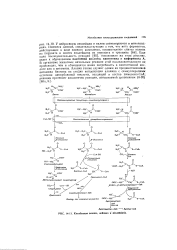 |
Катаболизм валина, лейцина и изолейцина. [28] |
У нейроспоры изолейцин и валин синтезируются в митохондриях. Еще одна последовательность реакций [65], показанная на этом рисунке, ведет к образованию пантоевой кислоты, пантетеина и кофермента А. В организме животных начальные реакции этой последовательности не происходят, чем и объясняется наша потребность в пантотеновой кислоте как в витамине. [29]
Но ингибитор изолейцин имеет мало общего с субстратом треонином. [30]
Страницы: 1 2 3 4