Менее стабильный изомер
Cтраница 2
Это, действительно, наблюдается в некоторых случаях: так, Майо и Вильцбах ( Mayo, Wilz-bach, 1949) показали, что цис - и / npawc - дихлорэтилены дают идентичные продукты с винил ацетатом. Отсюда следует, что в подобных случаях менее стабильный изомер должен быть более реак-ционноспособным. Действительно, менее стабильный транс - & и-хлорэтилен обладает большей реакционной способностью. Однако это положение в ряде случаев не оправдывается. Так, нитрилы малеиновой и фумаровой кислот не различаются по своей реакционной способности; хотя первый из них менее стабилен. Отсюда следует, что в приведенных примерах взаимное превращение образующихся радикалов протекает не одновременно с присоединением. Майо, Льюис и Уоллинг ( Mayo, Lewis, Walling, 1947) приписывают различие в реакционной способности, наблюдаемое в этих случаях, стерическому ингибированию резонанса. [16]
Поскольку происходит поглощение энергии, этот процесс не приводит к установлению термического равновесия. Однако можно достигнуть устойчивого состояния, при котором обычно преобладает менее стабильный изомер. [17]
К сожалению, полученные данные не имеют общего характера и их интерпретация, приведенная выше, является весьма упрощенной. В частности, стереохими-ческие результаты реакции восстановления ос р-ненасыщенных карбонильных соединении системой металл - донор протонов сильно зависят как от характера этой системы, так и от условий реакции. Более того, показано, что при восстановлении некоторыми системами образуется менее стабильный изомер. В данном случае вследствие диаксиального взаимодействия СН3 - СН30 в транс-декалоновых соединениях соответствующие производные г ис-декалина должны быть более стабильными, и тем не менее последние не образуются. Предполагалось [322], что стереохимия восстановления в данном случае определяется требованием наличия перекрывания орбитали пары электронов образующегося карбаниона с зт-орбиталями карбонильной группы. Для этого необходимо, чтобы орбиталь карбаниона была аксиальной, а не экваториальной. Последнее приводит к конечному продукту реакции с mpawc - сочленением колец. Следует отметить, что упомянутое выше утверждение, согласно которому свободная пара электронов занимает аксиальное положение, не оспаривается, однако предполагается, что причиной этого является скорее перекрывание орбиталей, чем пространственные требования свободной пары электронов. Очевидно, что этот новый аргумент непосредственно неприменим к стереохимии карбанионов, в которых отсутствует перекрывание орбиталей свободной пары электронов и карбонильной двойной связи. [18]
Некоторые реакции присоединения брома к диенам были изучены в условиях, когда известно, что продукт определяется кинетически контролируемой стадией. Так, Хатч и сотрудники [36] показали, что присоединение брома к бутадиену в ряде растворителей дает гранс-1 4-ди-бромбутен - 2 и 3, 4-дибромбутен - 1, причем первый образуется в значительно большем количестве. Таким образом, предпочтительным является 1 4-присоединение, приводящее к термодинамически менее стабильному изомеру. Как и в случае хлора, атака должна начинаться электрофильным бромом только по одной, а не по обеим двойным связям, поэтому с-1 4-аддукта в продукте реакции не было обнаружено. [19]
В табл. 14 представлены некоторые физические константы ряда цис - и транс-изомеров циклических систем: для чис-юомеров температура кипения, плотность и показатель преломления оказываются больше, чем для тра с-изомеров. Первыми на этот факт обратили внимание Ауверс и Скита [1], которые предположили, что такая картина изменения физических свойств имеет общее значение, и предложили использовать это явление для определения конфигурации изомеров. В более строгой формулировке правило Ауверса - Скита гласит, что большими температурой кипения, плотностью и показателем преломления обладает менее стабильный изомер. [20]
Замещение направляется н в положение 5, но образовавшийся продукт замещения быстро перегруппировывается по Боултону-Катрицкому в 7-сульфонилметилзамещенный продукт уже при обработке реакционной массы. При наличии 5 - или 7-метокситруппы влияние сульфоннлметнльной группы в заметной мере уравновешивается, перегруппировка Боултона-Катрицкого замедляется и за ней можно следить. Было установлено, что атака нуклеофила ( тозилметилхлорида), действительно, направляется по обоим положениям, 5 и 7, но термодинамически менее стабильный изомер в конце концов переходит практически полностью в более стабильный, а именно в тот, в котором рядом с нитрогруппои оказывается метоксигруппа как менее громоздкая. [21]
Замещение направляется н в положение 5, но образовавшийся продукт замещения быстро перегруппировывается по Боултону-Катрицкому в 7-сульфонилметилзамещенный продукт уже при обработке реакционной массы. При наличии 5 - или 7-метоксигруппы влияние сульфоннлметнльной группы в заметной мере уравновешивается, перегруппировка Боултона-Катрицкого замедляется и за ней можно следить. Было установлено, что атака нуклеофила ( тозилметилхлорида), действительно, направляется по обоим положениям, 5 и 7, но термодинамически менее стабильный изомер в конце концов переходит практически полностью в более стабильный, а именно в тот, в котором рядом с нитрогруппой оказывается метоксигруппа как менее громоздкая. [22]
Замещение направляется н в положение 5, но образовавшийся продукт замещения быстро перегруппировывается по Боултону-Катрицкому в 7-сульфонилметилзамещенный продукт уже при обработке реакционной массы. При наличии 5 - или 7-метокситруппы влияние сульфоннлметнльной группы в заметной мере уравновешивается, перегруппировка Боултона-Катрицкого замедляется и за ней можно следить. Было установлено, что атака нуклеофила ( тозилметилхлорида), действительно, направляется по обоим положениям, 5 и 7, но термодинамически менее стабильный изомер в конце концов переходит практически полностью в более стабильный, а именно в тот, в котором рядом с нитрогруппой оказывается метоксигруппа как менее громоздкая. [23]
Такое положение равновесия обозначают также как фотостационарное состояние. Положение равновесия определяется в первую очередь соотношением квантовых выходов обеих реакций. В общем случае справедливо, что при фотохимической изомеризации в отличие от термической ( Z) - ( E) - изомеризации равновесие смещено в сторону образования менее стабильного изомера. [24]
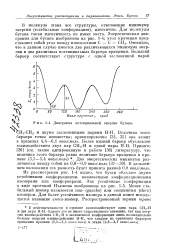 |
Диаграмма потенциальной энергии бутана. [25] |
Величина этого барьера точно неизвестна; ориентировочно [34, 35] она лежит в пределах 4 4 - 6 1 ккал / молъ. В дальнейшем изложении эта разность будет принята равной 0 8 ккал / молъ. Из рассмотрения рис. 1 - 4 видно, что бутан обладает двумя устойчивыми конформациями. Менее стабильный изомер называется гош - ( gauche) или скошенным ( skew) изомером. Для более устойчивого изомера в данной книге используется название анпш-изомер. [26]
Взаимопревращение чистых геометрических изомеров в равновесные смеси, содержащие оба изомера ( один из них нередко преобладает), хорошо известно в органической химии. Стереопревращения были осуществлены и при нагревании чистых изомеров. В настоящее время известно, что положение равновесия между двумя формами зависит от их относительной термодинамической устойчивости. Однако смеси, образующиеся при взаимопревращениях изомеров под влиянием облучения, часто в большем количестве содержат менее стабильный изомер. Часто для ускорения фотохимических стереопревращений применяются катализаторы; обычно они содержат элементы с высоким атомным весом, например бром и иод. [27]
Для эффективного сочетания таких соединений было предложено много методов, некоторые из них предусматривают использование солей тяжелых металлов, например соединений серебра или ртути, в качестве акцепторов кислоты. Гликозилгалогенид обычно используется в виде его ацетилированного производного и почти всегда получается из полностью ацетилированного сахара. Возможно существование двух аномерных форм гликозилгалогенидов, обычно называемых а - и р-производными, причем во многих случаях получаются одновременно оба аномера. Как показано в разд. Менее стабильный изомер можно получить в условиях кинетического контроля, и в ряде случаев это достигается при действии хлорида алюминия в холодном трихлорметане на подходящее производное сахара. [28]
Страницы: 1 2