Изотерма - ленгмюр
Cтраница 1
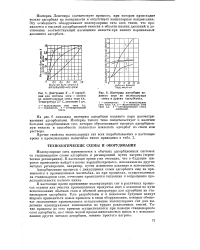 |
Диаграмма X - Y адсорбции для системы этан - этилен на молекулярных ситах типа 4А. Температура 25 С, давление i am.| Изотермы адсорбции водяного пара на молекулярных ситах и других адсорбентах. [1] |
Изотерма Ленгмюра соответствует процессу, при котором происходит только адсорбция на поверхности и отсутствует капиллярная конденсация. Эту особенность обнаруживают молекулярные сита всех типов, что проявляется в высокой адсорбционной емкости в области низких давлений и достижении соответствующей насыщению емкости при низких парциальных давлениях адсорбата. [2]
Изотерма Ленгмюра описывает процесс, при котором адсорбируемое вещество может занять лишь ограниченное число участков поверхности, причем каждый активный центр поверхности может сорбировать одну молекулу газа. [3]
Изотерма Ленгмюра широко используется для описания хемо-сорбционных равновесий, но опытные данные обычно указывают на ее неточность. Сопоставление теории с опытом проводится различными способами. [4]
Изотерма Ленгмюра довольно хорошо описывает адсорбционной поведение газов на различных поверхностях, и достоинство изотермы состоит в ее значительной простоте. Всего несколько задач в этой глапе будет посвящено этой изотерме, и они дадут представление о тех расчетах, которые могут быть сделаны. [5]
Изотерма Ленгмюра получается в предположении, что интенсивность сорбционного процесса пропорциональна концентрации раствора и числу незанятых мест для поглощающегося мигранта в твердой фазе, а7 интенсивность десорбции пропорциональна количеству поглощенного вещества. [6]
Изотерма Ленгмюра для двух газов, адсорбирующихся одновременно и без диссоциации на одном и том же адсорбенте, весьма полезна при истолковании результатов изучения каталитических реакций с участием двух веществ. [7]
Изотерму Ленгмюра легко получить, если принять, что в процессе сорбции поверхность адсорбента может покрываться только одним слоем адсорбата. Изотерма Фрейндлиха представляет собой чисто эмпирическое уравнение, но оно применяется во многих случаях, в особенности в радиохимии. [8]
Уравнение изотермы Ленгмюра описывает адсорбцию газов с четко выраженным насыщением. [9]
Форма изотермы Ленгмюра для некоторых значений / С показана на рис. 28.13. Покрытие поверхности увеличивается с давлением и приближается к единице только при очень высоких давлениях, когда газ эффективно прижимается к поверхности. При разных температурах получаются разные значения / С; вот почему этш линии называют изотермами. Отметьте, что / С является константой равновесия распределения вещества между поверхностью и газовой фазой. [10]
Форма изотермы Ленгмюра для некоторых значений / С показана на рис. 28.13. Покрытие поверхности увеличивается с давлением и приближается к единице только при очень высоких давлениях, когда газ эффективно прижимается к поверхности. При разных температурах получаются разные значения К; вот почему эти линии называют изотермами. Отметьте, что / ( является константой равновесия распределения вещества между поверхностью и газовой фазой. [11]
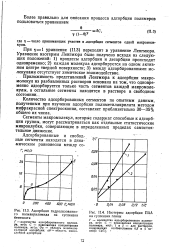 |
Изотермы адсорбции ПАА на суспензии глины. [12] |
Уравнение изотермы Ленгмюра было получено исходя из следующих положений: 1) процессы адсорбции и десорбции происходят одновременно; 2) каждая молекула адсорбируется на одном активном центре твердой поверхности; 3) между адсорбированными молекулами отсутствует химическое взаимодействие. [13]
Это - известная изотерма Ленгмюра, которая может быть получена совершенно строго самыми различными способами. [14]
Это - известная изотерма Ленгмюра, которая может быть получена со-першенно строго самыми различными способами. [15]
Страницы: 1 2 3 4