Изотерма - отклонение
Cтраница 1
Изотермы отклонения мольного обьема ( плотности), так же как и изотермы интенсивности рассеянного света, не являются симметричными относительно уровня исчезновения мениска. [1]
Изотермы отклонения от аддитивности могут быть положительными, отрицательными и S-образными. [2]
Экстремум изотермы отклонения вязкости от значений, рассчитанных в предположении отсутствия взаимодействия, так же как и в случае свойств, не подчиняющихся мольной аддитивности, смещается от точки стехиометрии, причем это смещение тем больше, чем меньше значение константы равновесия реакции обменного взаимодействия. [3]
 |
Диаграммы отклонения объемных свойств смешанных растворителей от аддитивности. [4] |
Как видно, изотермы отклонения всех свойств от аддитивности имеют экстремальный характер. [5]
Установлено, что изотермы отклонения интегральной интенсивности / полос поглощения от объемно-долевой аддитивности могут быть положительными, отрицательными и 5-образными. [7]
Рассмотрим главные особенности изотерм отклонения от аддитивности различных аддитивных свойств. Как было показано выше, экстремум на кривой истинномольного свойства ( 1 45) с изменением константы равновесия смещается от точки, отвечающей стехиометрии образующегося в системе соединения. Очевидно, что в этом случае и максимум отклонения истинномольного свойства от аддитивности также будет смещаться с изменением константы равновесия. [8]
Приведенные на рисунке изотермы отклонения молярного объема обеих систем имеют максимумы, соответствующие содержанию 3 ( 5) - метилпиразола в - 50 и 70 % мольн. [9]
Для системы ДЭГ МЭЭЭГ характерным является несиммет-ичность изотерм отклонения от аддитивности, а также сгла-сенность максимумов на изотермах. [10]
После того, как сравнительно подробно были разобраны особенности изотерм отклонения ст аддитивности объемных свойств, очевидно, не приходится специально останавливаться на опровержении последнего мнения. [11]
Анализ спектрофотометрических данных в системах с химическим взаимодействием проводится так же, как и в случае иных аддитивных свойств, по изотермам отклонения от аддитивности. [12]
Анализ на основании формулы ( 24) высотной зависимости отклонения мольного объема v ( h, t) ( а в силу уравнения ( 20) и отклонения плотности Ар) показывает: а) по мере приближения температуры системы к критической и непосредственной близости от уровня исчезновения мениска и при удалении по высоте от этого уровня вдоль изотермы наблюдается переход от линейной высотной зависимости к более плавной - с дробным показателем степени, который стремится к / з при р - - ph и T - Tk ( этот принципиальный результат требует тщательной экспериментальной проверки, так как он имеет непосредственное отношение к вопросу о форме критической изотермы [16]); б) с удалением температуры системы от критической линейный участок на изотермах отклонения мольного объема ( плотности) наблюдается на все большем перепаде высот по обе стороны от уровня исчезновения мениска, причем угловой наклон линейного участка, знание которого позволяет найти величину производной А, при этом уменьшается. [13]
 |
Свойства системы диоксан - вода. [14] |
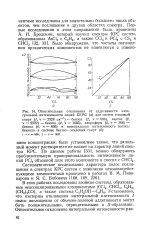
Расчет ре систем с взаимодействием показывает, что во всех случаях кривые этого свойства обладают экстремумом, точно или почти точно приходящимся на состав образующегося в системе продукта присоединения. На рис. 41 приводятся изотермы е и кривые ак и ре этой системы; на второй диаграмме этого рисунка приводятся изотермы отклонений экспериментальных значений т), п и мольного объема от значений, рассчитанных в предположении отсутствия взаимодействия. [15]
Страницы: 1 2