Изотерма - адсорбция - пар - бензол
Cтраница 1
Изотермы адсорбции паров бензола и к-гексана на окиси магния. [1]
На изотерме адсорбции пара бензола ( см. рис. 153) взята произвольная точка с координатами: РоЮ мм рт. ст., д0 0 262 кг / кг. [2]
На изотерме адсорбции пара бензола ( см, рис. 153) взята произвольная точка с координатами: Ро-10 мм рт. ст., а0 0 262 кг / кг. [3]
Основное отличие изотерм адсорбции паров бензола на каолините от изотерм на монтмориллоните состоит в том, что на каолините адсорбция обратима при любой температуре. С ростом температуры максимальная величина адсорбции несколько увеличивается, что обусловлено удалением сорбированной воды. [4]
На рис. 3 приведены изотермы адсорбции паров бензола, к-гексана и метанола на предельно алкоксилированных поверхностях рутила. По-видимому, проникшие сквозь разреженный алифатический частокол молекулы бензола вследствие стерических препятствий способны адсорбироваться лишь ребром. Молекулы же метанола во всех случаях проникают к поверхности ТЮ2 и как раз в количестве около 2 мкмоль / ма. Они способны образовать две водородные связи - с водородом Ti-ОН и с кислородом Ti-OR. He исключена возможность и химической реакции метанола с Ti-ОН, однако образующаяся при этом вода не в состоянии пробиться сквозь уже плотный частокол алифатических радикалов и в процессе откачивания образца при 150 С всегда будет гидролизовать поверхностный эфир, выделяя в объемную фазу более летучий из спиртов. Последний механизм может служить наглядным примером обратимой хемосорбции. [5]
На рис. 112 приведена изотерма адсорбции паров бензола на активной окиси алюминия. [6]
 |
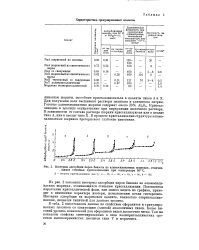
Изотермы адсорбции бензола на силикагеле КСК-2 при разных температурах, ( черные точки - десорбция. [7] |
На рис. 3 показаны изотермы адсорбции пара бензола на силикагеле при различных температурах. [8]
 |
Изотермы адсорбции паров бензола на алюмосиликатных гранулах, отличающихся степенью кристаллизации при температуре 80 С. [9] |
На рис. 2 показаны изотермы адсорбции паров бензола на алюмосили-катных шариках, отличающихся степенью кристаллизации. Постепенное нарастание кристаллической фазы, как можно видеть из графика, приводит к изменению характера изотерм, исчезновению петли гистерезиса. Изотерма адсорбции на шариковом цеолите, полностью откристаллизо-ванном, является типичной для данного цеолита. [10]
На рисунок нанесена также изотерма адсорбции паров бензола на этом же угле. [11]
Па рис. 26а сопоставлены изотермы адсорбции пара бензола па пени ристом грубодпсперспом кремнеземе ( дробленом кварце), на силпкэгелял. В области высоких давлений пара адсорбция на кварце остается обратимой ( чисто полпмо-лекуляриая адсорбция), а на силикагелях она сопровождается гистерезисом, ттшчным для капиллярной конденсации в открытых порах. Гост числа касаний глобул при обычной сушке уменьшает объем и размеры пор. [12]
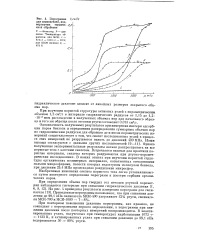 |
Порограмма. смЗ / г для силикагелей, подвергнутых термине - ffrff - ской обработке. [13] |
Однозначность полученных результатов при измерении изотерм адсорбции паров бензола и определении распределения суммарных объемов пор ло гидравлическим радиусам для образцов до и после порометрических измерений свидетельствует о том, что скелет исследованных углей в процессе этих измерений не разрушается вплоть до давлений 400 МПа. [14]
На рис. 1 и 2 приведены изотермы адсорбции паров бензола и воды на образцах А250 и ЭЗОО. Оба образца обладают, как это следует из рассмотрения изотерм, развитыми адсорбционными свойствами. Предельная величина поглощаемых паров как по бензолу, так и по воде практически одинакова и отвечает величинам 64 - 62 г и 72 - 73 г соответственно. Это указывает на одинаковый процент пористости указанных образцов. [15]
Страницы: 1 2