Изотерма - адсорбция - пар - бензол
Cтраница 2
 |
Расчетные показатели пористости, удельной поверхности скелета и среднего радиуса пор.| Кинетические показатели процесса восстановления КМЛПР. [16] |
На - основании полученных данных по изотермам адсорбции паров бензола рассчитаны пористость удельная поверхность скелета и средний радиус пор. [17]
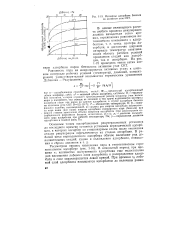 |
Изотермы адсорбции бензола на активном угле СК. Т. [18] |
На рис. 1 - 15 приведена такая сетка изотерм адсорбции паров бензола на активном угле СКТ. [19]
Параметры Wo, лсо и б могут быть рассчитаны из экспериментально измеренной изотермы адсорбции пара бензола в интервале P / P. [20]
Параметры W, х и 6 могут быть рассчитаны из экспериментально измеренной изотермы адсорбции пара бензола в интервале P / PS от 1 10 - 5 до 0 5 10 5 на ЭВМ. [21]
 |
Микрофотография диспергированных образцов гидроокиси магния. [22] |
А, поскольку их образование не сопровождается появлением гистерезиса на изотермах адсорбции пара бензола. [23]
В разделе III было показано, что объем микропор, вычисленный из изотермы адсорбции паров бензола по нижней границе области капиллярной конденсации меньше, чем объем микропор, найденный по f - методу, и в соответствии с этим удельная поверхность переходных пор, рассчитанная по поверхности жидкой пленки на стенках пор, больше, чем поверхность, найденная по - кривой. [24]
Допустим, требуется построить изотерму адсорбции пара ацетона при 30 С по известной изотерме адсорбции пара бензола при 20 С на том же поглотителе. На известной изотерме берут произвольную точку р и по рис. 11 непосредственно находят упругость пара р2 ацетона при 30 С. Следует, однако, иметь в виду: применение графика ограничено тем, что за известную изотерму, по которой строят изотермы адсорбции паров других веществ на том же поглотителе, должна быть принята только изотерма адсорбции пара бензола при 20 С. [25]
Допустим, по известной изотерме адсорбции паров бензола при 20 С ( кривая 1 6) требуется построить изотерму адсорбции паров этилового эфира при 0 С ( кривая 4 а) на том же поглотителе. [26]
Допустим, по известной изотерме адсорбции паров бензола при 20 С ( кривая 1 Ь) требует ся построить изотерму адсорбции паров этилового эфира при 0 С ( кривая 4 а) на том же поглотителе. [27]
Следует отметить, однако, что для оценки адсорбционных свойств силикагеля Хармадарьян и Копелевич пользовались величиной статической активности по бензолу, которая, как известно, не может полностью характеризовать пористую структуру. В дальнейшем, дополнив сведения об адсорбционной активности полученных ими си-ликагелей изотермами адсорбции паров бензола, авторы [38] пришли к выводу, что поглотительная способность зависит от объема пор и величины их радиусов. [28]
Допустим, требуется построить изотерму адсорбции пара ацетона при 30 С по известной изотерме адсорбции пара бензола при 20 С на том же поглотителе. На известной изотерме берут произвольную точку р и по рис. 11 непосредственно находят упругость пара р2 ацетона при 30 С. Следует, однако, иметь в виду: применение графика ограничено тем, что за известную изотерму, по которой строят изотермы адсорбции паров других веществ на том же поглотителе, должна быть принята только изотерма адсорбции пара бензола при 20 С. [29]
Рассмотрим вкратце вопрос о природе адсорбционных взаимодействий. Взаимодействия, характерные для сил, действующих между молекулами газов, являются универсальными. Они определяются поляризуемостью и магнитной восприимчивостью или потенциалом ионизации этих молекул, их размерами и рядом других их свойств. С этой точки зрения адсорбент должен был бы влиять одинаково на разные углеводороды, если указанные выше их физические свойства близки. Потенциалы ионизации и средние поляризуемости у бензола и гексана близки. Но если в случае адсорбции на чистом графите, не содержащем поверхностных окислов, в соответствии с несколько большими значениями потенциала ионизации и средней поляризуемости сильнее адсорбируется гексан, то на кварце исиликагеле наблюдается обратное: сильнее адсорбируется бензол. На рис. 1 показаны соответствующие абсолютные ( рассчитанные на единицу поверхности) изотермы адсорбции паров бензола и гексана на поверхности графита и гидратированной поверхности кварца. [30]
Страницы: 1 2