Изотерма - адсорбция - гиббс
Cтраница 1
Изотерма адсорбции Гиббса охватывает собой две кривые: 1) изотерму поверхностного натяжения как функцию концентрации af ( c) - кривая а, с 2) изотерму адсорбции - так же, как функцию концентрации TF ( c) - кривая Г, с. На рис. 64 представлена типичная форма этих кривых. [1]
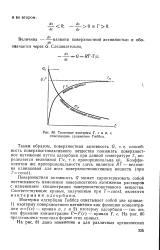 |
Типичные изотермы Г, с и сг, с, отвечающие уравнению Гиббса. [2] |
Изотерма адсорбции Гиббса охватывает собой две кривые: 1) изотерму поверхностного натяжения как функцию концентрации a f ( c) - кривая а, с и 2) изотерму адсорбции - так же, как функцию концентрации TF ( c) - кривая Г, с. На рис. 80 представлена типичная форма этих кривых. [3]
Уравнение изотермы адсорбции Гиббса с точки зрения термодинамики универсально и применимо к границам раздела любых фаз. Рассчитанные по этому уравнению значения Г наиболее близко совпадают со значениями, найденными другими методами, в области разбавленных растворов. [4]
Из уравнения изотермы адсорбции Гиббса следует, что в зависимости от знака производной da / dc направление процесса адсорбции может быть различным. Если же dt / dc 0, то Г8 0 и вещество не только не адсорбируется а, более того, отдаляется от поверхности тела. Это явление называют отрицательной адсорбцией, или десорбцией. [5]
Напишите уравнение изотермы адсорбции Гиббса, проанализируйте входящие в него величины, укажите условия и область применения. [6]
Это уравнение называют также изотермой адсорбции Гиббса. [7]
Для смесей неионногенных ПАВ и для индивидуальных ПАВ изотерма адсорбции Гиббса и уравнения Гиббса - Дюгема приводят к двум возможным причинам минимума межфазного натяжения в разбавленных системах: ( 1) изменения знака на поверхности раздела при избыточной концентрации ПАВ; ( 2) максимум химического потенциала ПАВ соответствует его общему содержанию. Какой из этих случаев реализуется в действительности, зависит от детального состава раствора, параметров адсорбции, распределения и образования ассоциатов, связанных уравнением сохранения массы. Специфические случаи были рассмотрены с помощью предела Бари - Хартли для многокомпонентных равновесий, а при рассмотрении смесей ПАВ использовали предел разделения фаз. В случае одного ПАВ, находящегося в двух фазах или в одной, обычно не наблюдается максимум химического потенциала. В случае двух ПАВ смешанные мицеллы должны образовывать по крайней мере одну фазу, что приводит к максимуму химического потенциала во всех исследованных случаях. [8]
Уравнение (11.21) называется обычно адсорбционной формулой Гиббса или изотермой адсорбции Гиббса. [9]
Уравнение ( IV, 8), называемое изотермой адсорбции Гиббса, используется для вычисления адсорбции. Уместно еще раз напомнить, что уравнение Гиббса применимо для плоской жидкой поверхности. [10]
Уравнение (11.21) называется обычно адсорбционной формулой Гиббса или изотермой адсорбции Гиббса. [11]
Термодинамические закономерности явлений в двойном электрическом слое, вывод которых основывается на изотерме адсорбции Гиббса, отнюдь не являются новым словом в науке, однако достаточная ясность в понимании указанных явлений приходила только постепенно. [12]
Сран-ский [215] и Сиерс [216] также предположили, что уменьшение свободной энергии поверхности или ступени в соответствии с изотермой адсорбции Гиббса может иметь важное значение. [13]
Уравнение ( 50 - 12) является аналогом соотношения Гиббса - Дюгема для поверхности и известно ( при dT Q) под названием изотермы адсорбции Гиббса. Согласно допущению Гиббса, связанный с поверхностью раздела объем равен нулю, так что т можно принять равным нулю. Однако Гуггенгейм предпочитает считать, что граница раздела фаз обладает ненулевой толщиной. В любом случае уравнение ( 50 - 12) справедливо независимо от выбора положения поверхности или поверхностей, определяющих границу раздела. [14]
Уравнение ( 50 - 12) является аналогом соотношения Гиббса - Дюгема для поверхности и известно ( при dT 0) под названием изотермы адсорбции Гиббса. Согласно допущению Гиббса, связанный с поверхностью раздела объем равен нулю, так что т можно принять равным нулю. Однако Гуггенгейм предпочитает читать, что граница раздела фаз обладает ненулевой толщиной. В любом случае уравнение ( 50 - 12) справедливо независимо от выбора положения поверхности или поверхностей, определяющих границу раздела. [15]
Страницы: 1 2