Изотерма - адсорбция - гиббс
Cтраница 2
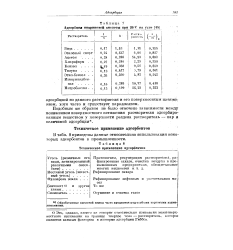 |
Адсорбция пикриновой кислоты при 20 на угле. [16] |
Это, однако, ничего не говорит относительно изменения межповерхностного натяжения на границе твердое тело - растворитель, которое является важным фактором в изотерме адсорбции Гиббса. [17]
Общая закономерность для всех хлоридов, как и дяя фторидов, согласно ЭКК заключается в том, что с увеличением температуры величина ( рн сдвигается в сторону более положи-телыых значений потенциалов, а значение 6mQx уменьшается, что соответствует изотерме адсорбции Гиббса. [18]
Здесь Г - избыточное содержание поверхностно-активного вещества на границе раздела фаз раствор - воздух; с - равновесная ( остаточная) концентрация ПАВ в растворе, а - поверхностное натяжение, R - газовая постоянная, Т - абсолютная температура. Обычно это выражение называют изотермой адсорбции Гиббса. [19]
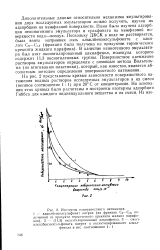
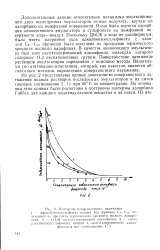
На рис. 2 представлены кривые зависимости поверхностного натяжения водных растворов исследуемых эмульгаторов и их смеси ( весовое соотношение 1: 1) при 20 С от концентрации. На основании этих кривых были расчитаны и построены изотермы адсорбции Гиббса для каждого индивидуального вещества и их смеси. [21]
На рис. 2 представлены кривые зависимости поверхностного натяжения водных растворов исследуемых эмульгаторов и их смеси ( весовое соотношение 1: 1) при 20 С от концентрации. На основании этих кривых были засчитаны и построены изотермы адсорбции Гиббса для каждого индивидуального вещества и х смеси. [23]
Адсорбция на твердой поверхности газообразных ( парообразных) и растворенных веществ зависит от концентрации. Чтобы описать количественную зависимость адсорбции от концентрации или давления, можно юобще использовать ранее выведенное уравнение изотермы адсорбции Гиббса, так как оно принципиально пригодно для любого конкретного случая. Однако практически для вычисления адсорбции на твердой поверхности использовать его не удается, так как шо содержит множитель da / dc, вычислить который нельзя из-за отсутствия методов прямого измерения поверхностного натяжения о твердых поверхностей. [24]
Это требование налагает ряд условий, которые определяют химический состав ( как объемный, так и поверхностный), объем и форму кристалла. Объемный состав кристалла задается единообразием химических потенциалов в различных частях объема; поверхностный состав связан с у ( п) изотермой адсорбции Гиббса. Теперь рассмотрим значение условий термодинамического равновесия для формы и объема кристалла. [25]
 |
Зависимость содержания золота. [26] |
Получены, однако, довольно надежные данные для близкого явления - обогащения одним из компонентов границ зерен сплава. При исследовании границ зерен вопрос о загрязнениях не стоит так остро, как в случае открытых поверхностей. Ввиду того что анализ данных основан на использовании изотермы адсорбции Гиббса, эти результаты относятся к весьма низкой концентрации растворенного вещества в объеме - обычно меньше 1 ат. [27]
В случае твердых тел дело обстоит не так просто. Отсутствуют точные методы определения их поверхностного натяжения, и нет методов измерения изменений этой величины. Проведя аналогию с жидкостями, Бенгхем с сотрудниками [31, 32] показал, что изотерма адсорбции Гиббса может быть применена к твердым телам. [28]
Термодинамическое рассмотрение поверх-постен раздела; изотерма адсорбции Гиббса. [29]
Страницы: 1 2