Изотерма - двуокись - углерод
Cтраница 1
Изотерма двуокиси углерода при Оа ( рис. 58) показывает разрыв ( точка Л) при давлении, когда начинается сжижение газа; сжижение продолжается до точки В. После этой точки, когда газ больше не существует, образовавшаяся жидкость сжимается линейно. Изотерма двуокиси углерода при 40 содержит только резко выраженный минимум. При этой температуре двуокись углерода остается газообразной до самых высоких давлений. [1]
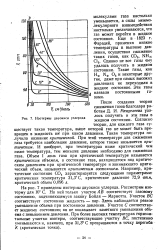 |
Изотермы двуокиси углерода. [2] |
На рис. Т приведены изотермы двуокиси углерода. Рассмотрим изотерму для 10 С. На ней только участок А В соответствует газовому состоянию, подчиняющемуся закону Бойля - Мариотта. Участок ВС соответствует состоянию жидкость - пар. Здесь наблюдается резкое уменьшение объема при постоянном давлении. Участок С соответствует жидкому состоянию; он не показывает заметного уменьшения объема с повышением давления. При более высоких температурах горизонтальные участки изотерм, соответствующие участку ВС, постепенно уменьшаются и, наконец, при 31 3 С превращаются в точку перегиба К. [3]
 |
Отклонения от законов идеальных газов. [4] |
На рис. 7 представлен ряд изотерм двуокиси углерода, экспериментально полученных Амага. Изотерма, отвечающая температуре 0 С, показывает, что сжатие углекислоты сопровождается уменьшением объема, и, когда давление и объем достигают значений, характеризуемых точкой а, дальнейшее уменьшение объема до точки в происходит без изменения давления. В последующем незначительное уменьшение объема требует весьма большого повышения давления. Аналогичный характер имеют изотермы 10 и 20, с той лишь разницей, что горизонтальные участки изотермы в а и в а становятся с понижением температуры все меньше, пока, наконец, при температуре 31 вырождаются в точку К, а при более высоких температурах совершенно исчезают. [5]
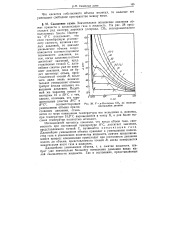 |
V - р - Изотермы СО2 по экспериментальным данным. [6] |
Значительное повышение давления может привести к конденсации газа в жидкость. На рис. 28 представлен ряд изотерм двуокиси углерода, С02, экспериментально полученных Амага. Изотерма 0 С показывает, что если газообразную углекислоту сжимать, начиная с малых давлений, то вначале уменьшение объема сопровождается соответствующим повышением давления, затем, когда давление и объем достигают значений, представляемых точкой С, дальнейшее сжатие уже не изменяет давления, пока не будет достигнут объем, представляемый точкой В, после чего даже очень незначительное уменьшение - объема требует весьма сильного повышения давления. [7]
Значительное повышение давления может привести к конденсации газа в жидкость. На рис. 28 представлен ряд изотерм двуокиси углерода, СОг, экспериментально полученных Амага. Изотерма 0 С показывает, что если газообразную углекислоту сжимать, начиная с малых давлений, то вначале уменьшение объема сопровождается соответствующим повышением давления, затем, когда давление и объем достигают значений, представляемых точкой С, дальнейшее сжатие уже не изменяет давления, пока не будет достигнут объем, представляемый точкой В, после чего даже очень незначительное уменьшение объема требует весьма сильного повышения давления. Подобный же характер имеют и изотермы 10 и 20 С с тем, однако, отличием, что горизонтальные участки В С и В С, соответствующие уменьшению объема при постоянном давлении, становятся по мере повышения температуры все меньшими и, наконец, при температуре 31 0 С вырождаются в точку К, а для более высоких температур полностью исчезают. [8]
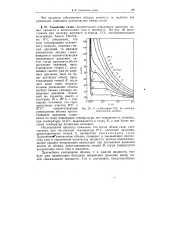 |
V - р - Изотермы СО2 по экспериментальным данным. [9] |
Значительное повышение давления может привести к конденсации газа в жидкость. На рис. 28 представлен ряд изотерм двуокиси углерода, СО2, экспериментально полученных Амага. Изотерма 0 С показывает, что если газообразную углекислоту сжимать, начиная с малых давлений, то вначале уменьшение объема сопровождается соответствующим повышением давления, затем, когда давление и объем достигают значений, представляемых точкой С, даль - нейшее сжатие уже не изме - t няет давления, пока не бу - ч дет достигнут объем, представляемый, точкой В, после чего даже очень незначительное уменьшение объема требует весьма сильного повышения давления. [10]
На рис. 7 представлен ряд изотерм двуокиси углерода, экспериментально полученных Амага. [11]
Значительное повышение давления может привести к конденсации газа в жидкость. На рис. 26 представлен ряд изотерм двуокиси углерода СО2, экспериментально полученных Амага. [12]
Значительное повышение давления может привести к конденсации газа в жидкость. На рис. 48 представлен ряд изотерм двуокиси углерода СО2, экспериментально полученных Амага. [13]
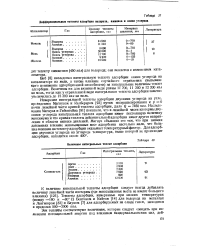 |
Дифференциальные теплоты адсорбции водорода, аммиака и окиси углерода. [14] |
Измерение интегральной теплоты адсорбции двуокиси углерода на угле, проведенное Магнусом и Келберером [93] путем экстраполирования к р О почти линейной части кривой теплоты адсорбции, дало Q 7450 кал. Исследования Магнуса и Гибенгейна [91] показали, что в линейной части изотермы двуокиси углерода интегральная теплота адсорбции имеет постоянную величину максимума и что кривая теплоты действительной адсорбции имеет другое направление в области низких - давлений. Магнус объяснял это тем, что при низких давлениях влияние ненасыщенных мест адсорбента настолько мало, что большее влияние на теплоту адсорбции оказывает температурный фактор. [15]
Страницы: 1 2