Любая изотерма
Cтраница 1
 |
Фазовая диаграмма многокомпонентной углеводородной смеси. [1] |
Любая изотерма, проведенная с расчетом пересечения области обратной конденсации ( например, изотерма Za), в точке касания к одной из изолиний процентного содержания жидкости в смеси показывает возможное максимальное образование конденсата для данных температуры и давления. [2]
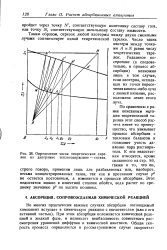 |
Определение числа теоретических тарелок на диаграмме теплосодержание - состав. [3] |
Таким образом, отрезок любой изотермы между двумя смежными лучами соответствует одной теоретической тарелке. [4]
Если температура ниже критической, то любая изотерма имеет три характерных участка. [5]
В принципе уравнение (2.33) справедливо для любой изотермы и поэтому позволяет количественно описать динамику, контролируемую смешанно-диффузионной кинетикой в самом общем виде. Однако реализация этого принципа требует решения интег-родифференциальных уравнений в частных производных. Поэтому вместо уравнения (2.33) обычно изыскиваются эквивалентные ему приближенные выражения, на основе которых можно было бы сделать полуколичественные, но зато более общие заключения. [6]
Имеет третий порядок относительно объема V, любая изотерма при параметрах состояния, меньших критич. Наиб, из корней ур-ния соответствует газовой фазе, наименьший - жидкой; средний корень ур-ния физ. [7]
Поскольку уравнение Ван-дер - Ваальса является кубическим относительно объема, то любая изотерма в докритических условиях имеет один или три действительных положительных корня, в то время как сверхкритические изотермы ( см. рис. 4.1, кривая 3) имеют лишь один действительный положительный корень. [8]
Кривая, отражающая правую часть уравнения ( 25), для любой изотермы асимптотически приближается к некоторой величине Г, которая зависит от вида изотермы. [9]
В этом случае внутренний коэффициент массоотдачи Р Рп - Уравнение ( II 1.87) справедливо для любой изотермы адсорбции. Если же внутреннее сопротивление зависит как от диффузии в порах, так и от диффузии в сорбенте или на его внутренней поверхности, то строгая связь между коэффициентами массоотдачи и массопередачи существует лишь для линейной изотермы адсорбции. [10]
В качестве объемной функции р можно принять значения AZ Z - txo - iO - на любой изотерме, но для усреднения была принята функция, равная сумме AZj на всех изотермах [15] выше 110 К. Разделив значения AZ, насчитанные по опытным данным [2, 15 - 18] на р, согласовав и сгладив полученные результаты, получим значения температурной функции в интервале температур 110 - 673 15 К. По выделенным элементарным функциям ао, 1, Р it э были найдены значения второго вариального коэффициента В. [11]
 |
Изотермы вблизи критической точки Т.| Общий вид фазовой диаграммы ( гипотетический. [12] |
Если на фазовой диаграмме изобразить кроме устойчивых и метастабильные жидкие и газообразные состояния вещества, то изотермы будут располагаться так, как показано на рис. 3.17. В каждой из точек любой изотермы, за исключением точек, лежащих между В и С, вещество находится в однородном состоянии. Следовательно, точки В и С представляют собой предельные однородные состояния вещества. Равновесный фазовый переход начинается в точке А или D прямолинейного участка изотермы. [13]
Если на фазовой диаграмме изобразить кроме устойчивых еще и метастабильные жидкие и газообразные состояния вещества, то изотермы будут располагаться так, как показано на рис. 4.16. В каждой из точек любой изотермы, за исключением точек, лежащих между В и С, вещество находится в однородном состоянии. В точках В и С ( др / ди) т 0; следовательно, точки В и С представляют собой предельные однородные состояния вещества. [15]
Страницы: 1 2
