Любая изотерма
Cтраница 2
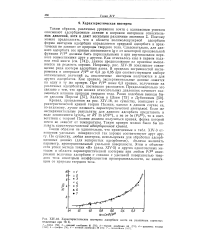 |
Характеристические изотермы адсорбции азота на различных пористых веществах при 78 К. [16] |
Таким образом не удивительно, что приведенные в табл. XIV-3 отношения удельных поверхностей так хорошо соответствуют друг другу. По существу, любая изотерма, используемая для обработки адсорбционных данных ( для непористых адсорбентов), должна включать параметр, пропорциональный удельной поверхности. Этим и объясняется успех метода точки 5 ( разд. XIV-5) и других одноточечных методов: в области характеристической изотермы при любом Р / Р измеряемая величина адсорбции v связана с удельной поверхностью твердого тела некоторым коэффициентом пропорциональности, не зависящим от природы твердого тела. [17]
Подставляя в (11.78), (11.79) или (11.80) уравнение любой изотермы адсорбции, отличной от лангмюровской, получаем измененные кинетические зависимости, характеризующие процесс на неоднородной поверхности или при взаимодействии молекул в адсорбированном слое. Если адсорбционное равновесие не достигается, соответствующие неравновесные зависимости получают, заменяя уравнения изотерм адсорбции зависимостями степеней заполнения поверхности от концентраций реагентов в объеме, определенными из условия баланса потоков адсорбции, собственно реакции и десорбции. [18]
Видно, что кривые распределения веществ для линейной и выпуклой изотерм имеют существенно разный вид. Рассмотренный ступенчатый метод решения задачи диффузии в сорбирующей среде может быть распространен на любую изотерму сорбции. [19]
При невыполнении одного из постулатов Лангмюра ( см. раздел 1.2) вид изотермы адсорбции меняется. Подставляя в формулы (11.88) - (11.90) уравнение любой изотермы адсорбции, отличной от лангмюровской, получаем видоизмененные кинетические зависимости, характеризующие процесс на неоднородной поверхности или при взаимодействии молекул в адсорбированном слое. Если адсорбционное равновесие не достигается, соответствующие неравновесные зависимости получают, заменяя уравнения изотерм адсорбции зависимостями степеней заполнения поверхности от концентраций реагентов в объеме, определенными из условия баланса потоков адсорбции, собственно реакции и десорбции. [20]
 |
Процесс ректификации на - диаграмме. [21] |
Схема процесса ректификации изображена на рис. 5.4. Здесь в координатах t, линиями / 7 и Ж показаны равновесные кривые пара и жидкости при давлении в генераторе рк. Ось координат направлена вниз по направлению возрастания температуры в ректификаторе. Точки пересечения кривых Я и Ж с любой изотермой ( горизонтальной прямой) показывают равновесные концентрации пара и жидкости при данной температуре. [22]
Предсказываемая уравнением ( 71) линейная зависимость емкости от количества адсорбированного вещества проверялась Парсон-сом в 1959 г. [70] в связи с формой адсорбционной изотермы. Однако можно показать, что в области потенциалов, где адсорбционной емкостью в уравнении ( 70) можно пренебречь ( т.е. в окрестности Емакс), соотношение ( 71) справедливо для любой изотермы, снятой при постоянном потенциале. Тип изотермы становится важным лишь в области десорбционных пиков, положение и форма которых определяются изотермами адсорбции через адсорбционную емкость. Теоретические представления о форме десорбционных пиков подробно рассматривались Фрумкиным и сотрудниками. [23]
Обычно в экспериментальных условиях непосредственно измеряется концентрация с. Если условия опыта таковы, что концентрация с в течение опыта поддерживается постоянной, задача легко решается методом разделения переменных для любой изотермы сорбции. [24]
Некоторые изотермы этого типа были изображены на рис. 7 для изученной Райер-соном и Камероном [18] адсорбции брома на силика-геле. Брунауер и Эммет [7.] измерили адсорбцию семи различных газов на двух образцах силикагеля, переданного им Райерсоном. Так как п относительно велико, то не будет серьезной ошибки, если положить п-оо и пользоваться при обработке данных Райерсона и Камерона простым уравнением ( 38), содержащим две константы. Другое упрощающее предположение касается константы с. Райерсон и Камерон вычислили по уравнению Клау-зиуса - Клапейрона [ гл. Это значение представляет, однако, теплоту адсорбции при образовании лишь части мономолекулярного слоя, и величина Е1 - средняя теплота адсорбции для всего первого слоя - может быть меньше этого значения. Если это верно, то из уравнения ( 38) следует, что vvm при / 0 5р0, и следовательно, константа vm может быть найдена из любой изотермы. Если вычислять величину поверхности, покрытой молекулами брома, исходя из плотности жидкого брома, то для удельной поверхности силикагеля получается значение 470л2 / з, что находится в превосходном согласии с величиной 500 м / г, найденной из изотерм типа / / для азота, аргона, кислорода, окиси углерода и сернистого газа, рассмотренных в предыдущем разделе. [25]
При е 1, или Е, EL уравнения ( 38) и ( 41) описывают изотермы типа III. Некоторые изотермы этого типа были изображены на рис. 7 для изученной Райер-соном и Камероном [18] адсорбции брома на еилика-геле. Брунауер и Эммет [7] измерили адсорбцию семи различных газов на двух образцах силикагеля, переданного им Райерсоном. Так как п относительно велико, то не будет серьезной ошибки, если положить поо и пользоваться при обработке данных Райерсона и Камерона простым уравнением ( 38), содержащим две константы. Другое упрощающее предположение касается константы с. Райерсон и Камерон вычислили по уравнению Клау-зиуса - Клапейрона [ гл. Это значение представляет, однако, теплоту адсорбции при образовании лишь части мономолекулярного слоя, и величина Ег - средняя теплота адсорбции для всего первого слоя - может быть меньше этого значения. Если это верно, то из уравнения ( 38) следует, что v - vm при р0 5р0, и следовательно, константа vm может быть найдена из любой изотермы. Если вычислять величину поверхности, покрытой молекулами брома, исходя из плотности жидкого брома, то для удельной поверхности силикагеля получается значение 470 л 2 / г, что находится в превосходном согласии с величиной 500 л 2 / г, найденной из изотерм типа / / для азота, аргона, кислорода, окиси углерода и сернистого га. [26]
Страницы: 1 2