Парциальная изотерма - адсорбция
Cтраница 1
Парциальные изотермы адсорбции, рассчитанные при постоянном молярном объеме одного из компонентов и увеличении молярного объема другого компонента от 0 09 до 0 15 дм3 / моль, приведены на рис. 5.16. Сравнивая рис. 5.16 / и 5.16 / /, можно сделать вывод, что увеличение молярного объема второго компонента сильнее понижает парциальные изотермы адсорбции обоих компонентов, чем увеличение молярного объема первого компонента. [1]
Для расчета парциальной изотермы адсорбции условного компонента из смеси необходимо также знать величину ( V / - - КН2о) / УИ, выраженную в см3 / ед. Для многих веществ, принадлежащих к различным классам органических соединений, величины 6 имеют очень близкие значения - в среднем б 0 373 - 10 - 3 см3 / ед. [2]
Это - уравнение парциальной изотермы адсорбции, поскольку оно связывает равновесные величины адсорбции данного компонента с его равновесной концентрацией. [3]
Уравнения (V.25) и (V.26) являются уравнениями парциальной изотермы адсорбции одного из органических компонентов и изотермы адсорбции воды из трехкомпонентного раствора, состоящего из смеси двух органических веществ, растворенных в воде. [4]
Уравнение ( 5) представляет собой общее уравнение парциальных изотерм адсорбции бинарных газо. [5]
Полученные обобщенные значения параметра 6 дают возможность рассчитать парциальную изотерму адсорбции неизвестного компонента из смеси с веществом известного строения а затем суммарную изотерму адсорбции этой смеси. Такие расчеты были проверены на модельных смесях двух веществ, одно из которых было использовано в качестве условного компонента. [6]
Полученные обобщенные значения параметра, 6 дают возможность рассчитать парциальную изотерму адсорбции неизвестного компонента из смеси с веществом известного строения, а затем суммарную изотерму адсорбции этой смеси. Такие расчеты были проверены на модельных смесях двух веществ, одно из которых было использовано в качестве условного компонента. Модельными системами при молярном соотношении С02: Со1 1: 1 служили следующие смеси: п-хлоранилин - нитробензол; - нитрофенол - нитробензол; диметилацетамид - изобутиловый спирт. [7]
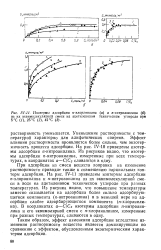 |
Изотермы адсорбции л-хлоранилина ( а и л-нитроанилина ( 6 из их эквимолекулярной смеси на ацетиленовом техническом углероде при 5 С ( i 25 C ( 2, 42 С ( 3. [8] |
При адсорбции из смеси веществ поправка на изменение растворимости приводит также к совмещению парциальных изотерм адсорбции. На рис. IV-11 приведены изотермы адсорбции п-хлоранилина и и-нитроанилина из их эквимолекулярной смеси в воде на ацетиленовом техническом углероде при разных температурах. В координатах а - CjCs изотермы адсорбции л-нитроани-лина и его эквимолярной смеси с л-хлоранилином, измеренные при разных температурах, сливаются в одну. [9]
Изотерму, характеризующую распределение каждого компонента между адсорбционной фазой и раствором, называют парциальной изотермой адсорбции, а изотерму, характеризующую распределение обоих компонентов ( растворенного вещества и растворителя) между адсорбентом и раствором, изотермой избирательной адсорбции. [10]
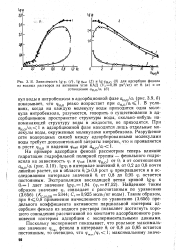 |
Зависимость Igcp, ( /, lgcp 36 ( 2 и lgcpH2o ( 3 Для адсорбции фенола из водных растворов на активном угле КАД ( Ка0 38 дм3 / кг от 0, ( а и от. [11] |
Таким образом, при 9 0 8 применение вычисленного по уравнению (3.656) предельного коэффициента активности парциальной изотермы адсорбции фенола из водного раствора позволяет достигнуть хорошего совпадения рассчитанной по константе адсорбционного равновесия изотермы адсорбции с экспериментальными данными. [12]
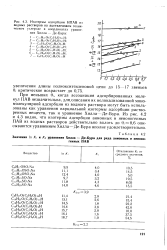 |
Изотермы адсорбции НПАВ из водных растворов на ацетиленовом техническом углероде в координатах уравнения Хилла - Де-Бура. [13] |
При меньших в /, когда ассоциация адсорбированных молекул ПАВ незначительна, для описания их нелокализованной мономолекулярной адсорбции из водного раствора могут быть использованы как уравнения парциальной изотермы адсорбции растворенных веществ, так и уравнение Хилла-Де - Бура. Из рис. 4.2 и 4.3 видно, что изотермы адсорбции анионных и неионогенных ПАВ из водных растворов действительно вплоть до 8, 0 б описываются уравнением Хилла-Де - Бура вполне удовлетворительно. [14]
При меньших 0 /, когда ассоциация адсорбированных молекул ПАВ незначительна, для описания их нелокализованной мономолекулярной адсорбции из водного раствора могут быть использованы как уравнения парциальной изотермы адсорбции растворенных веществ, так и уравнение Хилла-Де - Бура. Из рис. 4.2 и 4.3 видно, что изотермы адсорбции анионных и неионогенных ПАВ из водных растворов действительно вплоть до 0, 0 6 описываются уравнением Хилла-Де - Бура вполне удовлетворительно. [15]
Страницы: 1 2