Парциальная изотерма - адсорбция
Cтраница 2
Радке и Прауснитц [151] используя данные работы [149] о том, что при адсорбции смеси паров поверхностные бинарные растворы вдоль линии постоянного двумерного давления являются идеальными и к ним применим закон Рауля, сделали попытку вычисления парциальных изотерм адсорбции отдельных органических веществ из их смеси в разбавленных водных растворах. [16]
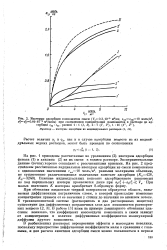
Парциальные изотермы адсорбции, рассчитанные при постоянном молярном объеме одного из компонентов и увеличении молярного объема другого компонента от 0 09 до 0 15 дм3 / моль, приведены на рис. 5.16. Сравнивая рис. 5.16 / и 5.16 / /, можно сделать вывод, что увеличение молярного объема второго компонента сильнее понижает парциальные изотермы адсорбции обоих компонентов, чем увеличение молярного объема первого компонента. [17]
Изложена строгая теория адсорбции бинарных газовых смесей на языке термодинамических вакансионных растворов. Выведены уравнения для парциальных изотерм адсорбции и для теплот адсорбции. [18]
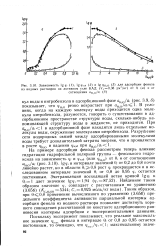 |
Зависимость Ig ср, ( /, lg ( р. 6 ( 2 и Ig pH2o ( - 3 Для адсорбции фенола из водных растворов на активном угле КАД ( Ка0 38 дм / кг от 0 - ( а и от. [19] |
Igip / в интервале значений 6, от 0 2 до 0 8 почти линейно растет, но в области в 0 8 рост ф / прекращается и в исследованном интервале значений 6, от 0 8 до 0 95 ф, остается постоянным. Таким образом, при 6 0 8 применение вычисленного по уравнению (3.656) предельного коэффициента активности парциальной изотермы адсорбции фенола из водного раствора позволяет достигнуть хорошего совпадения рассчитанной по константе адсорбционного равновесия изотермы адсорбции с экспериментальными данными. [20]
Складывается противоречивая ситуация: то что считалось и считается естественным для реальных адсорбентов ( неоднородность поверхности), с нашей точки зрения, оказывается нереальным; ближе к истине представление об однородности поверхности реальных адсорбентов или в общем случае об их дискретной однородности. Под последним подразумевается наличие в адсорбенте небольшого числа чем-то различающихся однородных поверхностей, для каждой из которых существуют своя постоянная энергия адсорбции и своя парциальная изотерма адсорбции. [21]
На рис. 1 приведены рассчитанные по уравнениям ( 2) изотермы адсорбции фенола ( 1) и анилина ( 2) из их смеси в водном растворе. Экспериментальные данные ( точки) хорошо совпадают с рассчитанными кривыми. На рис. 2 представлены рассчитанные парциальные изотермы адсорбции из смеси компонентов с одинаковыми значениями с. Влияние индивидуальных констант адсорбционного равновесия на ход парциальных изотерм проявляется даже при aai - f - azv; Fa. При малых значениях К изотерма приобретает S-образную форму. [23]
В докладе высказывается принципиально новая точка зрения, согласно которой то, что считалось и считается естественным для реальных адсорбентов ( неоднородность адсорбентов), с нашей точки зрения оказывается нереальным. Под последней подразумевается наличие в адсорбенте небольшого числа чем-то различающихся однородных поверхностей, для каждой из которых существует своя постоянная энергия адсорбции и своя парциальная изотерма адсорбции. Точка зрения автора уже по самой формулировке противоречива. Ведь различающиеся однородности являются, по существу, ни чем иным, как неоднородностью энергетической, а то, что их небольшое число, сути дела не меняет. [24]
Можно заметить, что значение К2 несколько уменьшается с ростом длины полиоксиэтильной цепи в молекуле НПАВ. При адсорбции анионных ПАВ колебания значения К-2 находятся, по-видимому, в пределах ошибки опыта. Значения Кз больше единицы, указывают на существование заметного взаимного притяжения молекул в адсорбционном слое [120], тогда как (, 1 в уравнении парциальной изотермы адсорбции растворенного вещества характеризует интенсивность ван-дер-ваальсовских сил отталкивания между адсорбированными молекулами, в значительной мере вызванных взаимодействием одинаково ориентированных на границе раздела фаз диполей. [25]
Страницы: 1 2