Критическая изотерма
Cтраница 2
С возрастанием температуры выше критической изотермы постепенно принимают вид плавных кривых, напоминающих изотермы идеального газа. [16]
Точка С на критической изотерме ( см. рис. 4.1, кривая 2) обозначает критическую точку. Соответствующие этой точке координаты ( рс, vc) являются критическими давлением и объемом. Эта точка характеризуется равенством нулю первой и второй производной давления по объему при критических температуре и объеме. [17]
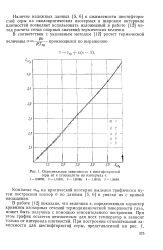 |
Относительная зависимость е шестифтор истой серы от е углекислоты на изотермах т. [18] |
Комплекс Окр на критической изотерме выделен графически путем построения изохор а по данным [5, 6] и увязки их с кривой насыщения. [19]
Предельная изотерма называется критической изотермой, и температура, ей соответствующая, называется критической температурой. Таким образом, при температурах выше критической вещество ни при каких давлениях не может быть переведено из газообразного состояния в жидкое. Эти газы характеризуются очень низкими критическими температурами, которые были недостижимыми для того времени, когда устанавливалась эта терминология. [20]
Проходящая через критическую точку критическая изотерма является предельной изотермой двухфазной области, у которой прямолинейный участок вырождается в точку. Значит, точка К ( рис. 1 - 1) является для критической изотермы точкой перегиба. [21]
Проходящая через критическую точку критическая изотерма является предельной изотермой двухфазной области, у которой прямолинейный участок вырождается в точку. Значит, точка К является для критической изотермы точкой перегиба. [22]
Другой важной характеристикой является критическая изотерма. [23]
Первая формула определяет характер критической изотермы, вторая - поведение поверхностного натяжения М вблизи критической точки. [24]
В области, лежащей выше критической изотермы и правее кривой ВК, двухфазное состояние невозможно, и с ростом температуры и объема изотермы приближаются по форме к изотермам идеального газа PV const. [25]
Если сжатие вести по критической изотерме t tK, то она не пересечет пограничные NK и МК, а только коснется их критической точки. Изотермы с температурами выше критической проходят выше точки К, имея здесь перегиб, который будет тем меньше, чем выше температура перегретого пара над уровнем критической температуры тела, тем больше газ по своим свойствам приближается к свойствам идеального газа. [26]
На рис. 213 показаны также критическая изотерма и две изотермы, соответствующие температурам выше критической. [27]
 |
Диаграмма Т - S для воздуха. [28] |
Вся верхняя часть диаграммы от критической изотермы и выше соответствует состоянию постоянных газов. [29]
Мы видели уже, что ниже критической изотермы расположена область равновесия жидкости и пара, где изотермы, построенные по уравнению Ван-дер - Вальса, пересекаются с изобарами, отвечающими равновесию, в трех точках. Здесь, следовательно, для соответственно выбранных значений температуры и давления все три корня рассматриваемого уравнения являются вещественными и неодинаковыми. Близ критического состояния численные значения корней мало отличаются друг от друга, и в критической точке они совпадают. [30]
Страницы: 1 2 3 4