Критическая изотерма
Cтраница 4
Геометрически критическая точка представляет собой точку перегиба критической изотермы. [46]
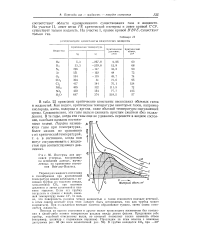 |
Изотермы для двуокиси углерода, построенные на основании данных, вычисленных по уравнению состояния Ван-дер - Ваальса. [47] |
На участке II, левее ветви РЕ критической изотермы и левее кривой С СР, существует только жидкость. На участке I, правее кривой В ВРЕ, существует только газ. [48]
Для любых составов бинарной системы справа от критической изотермы и вне области двухфазного равновесия смесь находится в газовом состоянии. Если температура ниже критической, то вне двухфазной области смесь находится в жидком состоянии. [49]
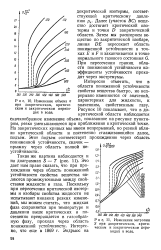 |
Изменение объема v при докритическом, критическом и закритическом переходах в воде.| Изменение энтропии. [50] |
Далее ( участок ВС) вещество достигает критической изотермы и точки D закритической области. Затем мы расширяем вещество по закритической изобаре, линия DE пересекает область пониженной устойчивости в точках Е и F и заканчивается в точке нормального газового состояния G. При пересечении границ области пониженной устойчивости коэффициенты устойчивости проходят через экстремумы. [51]
Изотерму, содержащую критическую точку, называют критической изотермой. При температурах, превышающих критическую, образование жидкости уже невозможно. [52]
Изотерма, соответствующая критической температуре, называется критической изотермой. [53]
Изотерма, содержащая точку перегиба, называется критической изотермой, а соответствующая ей температура Ге - критической температурой. Объем Vc и давление рс точки перегиба, в которой горизонтальная касательная, называются критическим объемом и критическим давлением. Состояние, соответствующее Vc, pc, Тс, называется критическим состоянием или критической точкой системы. [54]
Из диаграммы следует, что в точке К критическая изотерма имеет характерный перегиб. При температурах t tK изотермы углекислоты весьма близки к изотермам идеального газа. [55]
Из термодинамики критических явлений [1] известно, что критическая изотерма - изобара химического потенциала компонента двойного раствора является кривой нечетного порядка и имеет в критической точке точку перегиба с горизонтальной касательной. Следовательно, вблизи критической точки критическая изотерма парциального давления имеет горизонтальный участок, где парциальное давление практически не зависит от состава. Естественно, что критическая изотерма общего давления является также кривой нечетного порядка и имеет в критической точке нулевое значение первой и второй производных от давления по составу. [56]
Представляет значительный интерес установление вида критической изохоры и критической изотермы в области критической точки. [57]
Страницы: 1 2 3 4