Равновесная изотерма - адсорбция
Cтраница 1
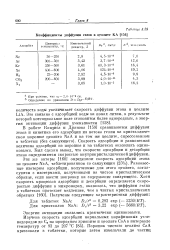 |
Коэффициенты диффузии газов в цеолите К А. [1] |
Равновесные изотермы адсорбции, полученные для этого цеолита, согласуются с изотермами, полученными на чистом кристаллическом образце, если ввести поправку на содержание связующего. [2]
 |
Равновесная адсорбция на активированном угле. [3] |
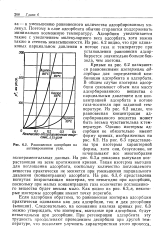
Кривые на рис. 6.2 называются равновесными изотермами адсорбции для определенной комбинации адсорбента и адсорбата. В общем случае изотерма адсорбции связывает объем или массу адсорбированного вещества с парциальным давлением или концентрацией адсорбата в потоке газа-носителя при заданной температуре. Из рис. 6.2 видно, что равновесная концентрация адсорбированного вещества может быть весьма чувствительна к температуре. [4]
Чтобы описать адсорбционные свойства активного колумбийского угля LCK, были определены равновесные изотермы адсорбции. К адсорбату, концентрация которого изменялась от колбы к колбе, добавляли одинаковое количество угля - 0 2 г, исключением были эксперименты с 2 4-динитрофено-лом, когда было добавлено только 0 1 г активного угля. Разные концентрации адсорбата достигались разбавлением исходного раствора дистиллированной водой. При этом концентрация адсорбата изменялась в пределах всего диапазона, представляющего интерес для исследования. [5]
Второй способ определения удельной поверхности из несимметричных пиков требует определения из хроматограммы равновесной изотермы адсорбции, как описано выше ( см. стр. [6]
Однако строго это уравнение справедливо только в случае линейной идеальной хроматографии, когда равновесная изотерма адсорбции линейна, скорость установления адсорбцион-но-десорбционного равновесия бесконечно большая и процессы диффузии в колонне не происходят. В этом случае профиль введенной в колонну полосы ( начального пика) адсорбата не изменяется при прохождении через колонну. В действительности при перемещении хроматографического пика вдоль колонны процессы адсорбции и десорбции происходят с конечной скоростью. Кроме того, при этом происходят разные виды диффузии. [7]
 |
Сравнение теории с данными Кэссиди и Вуда для лауриновой кислоты на активированном угле. [8] |
В работах [10-12] было показано, что экспериментальные выходные кривые С02, С2Н4 и С3Нв на силикагеле соответствуют равновесным изотермам адсорбции, измеренным предварительно независимым методом. [9]
Если среднее время жизни адсорбированного иона ПАВ меньше среднего времени жизни иона, локализованного в силовом поле мицеллы, то на равновесных изотермах адсорбции наблюдается максимум, обусловленный как бы разрушением адсорбционного слоя. [10]
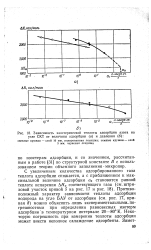 |
Зависимость изостерической теплоты адсорбции азота на. [11] |
Противоположный характер зависимости теплоты адсорбции водорода на угле БАУ от адсорбции ( см. рис. 17, кривая 8) можно объяснить лишь экспериментальными-погрешностями при определении равновесных изотерм адсорбции в температурном интервале 20 - 80 К. Некоторую погрешность при измерении теплоты адсорбции может внести неполное охлаждение адсорбента. [12]
CaKG внутрикристаллическое пространство практически полностью доступно молекулам Н20, N2 и СН3ОН, в то же время молекулы С2Н5ОН и С3Н7ОН диффундируют в полости цеолитов чрезвычайно медленно и даже за длительное время не удается получить равновесные изотермы адсорбции. [13]
В реальной практике крашения такой процесс адсорбции наиболее близко отвечает крашению гидрофобных синтетических волокон дисперсными красителями. Равновесные изотермы адсорбции в этом случае имеют линейный вид, и коэффициент распределения красителя между фазами волокна и раствора является величиной постоянной, численно равной тангенсу угла наклона таких прямых. Однако такой процесс с равным успехом можно относить и к типично адсорбционным, когда степень насыщения волокна молекулами дисперсного красителя очень невысока. Краситель в волокне удерживается силами Ван-дер - Ваальса, водородными связями и ди-поль-дипольным взаимодействием. [14]
На рис. 1 приведены полученные нами кинетические изотермы цикло-гексана на активном угле суперсорбон. Если считать, что равновесные изотермы адсорбции в этом случае могут быть описаны уравнением Дубинина - Радушкевича, то из данных, приведенных на рис. 1, могут быть вычислены константы этого уравнения W0 и В, которые, конечно, не зависят от температуры. [15]
Страницы: 1 2