Равновесная изотерма - адсорбция
Cтраница 2
В теории равновесной хроматографии предполагается, что в газо-хроматографических опытах соблюдаются условия, позволяющие пренебречь диффузионным и кинетическим размыванием хромато-графической полосы. Искажение полосы объясняется только отклонением равновесной изотермы адсорбции от изотермы Генри. Количественная связь равновесной изотермы ( распределения между подвижной и неподвижной фазами) и равновесной хроматограммой рассмотрены во многих обзорах 48 - 5В, поэтому здесь будет изложен только метод Глюкауфа В1 применительно к газоадсорбционной хроматографии. [16]
В теории равновесной хроматографии предполагается соблюдение условий, практически устраняющих диффузионное и кинетическое размывание хроматографической полосы. Поэтому форма хроматографического пика определяется только равновесной изотермой адсорбции. [17]
В таком случае их парциальное давление в колонке составляет малую долю давления их пара, и равновесная изотерма адсорбции еще очень близка к своей касательной, проведенной через начало координат. В то же время наклон этой касательной очень велик и коэффициенты емкости колонки остаются приемлемыми. В случае анализа более высококи-пящих соединений отклонение изотермы адсорбции от линейности при парциальных давлениях, обычно достигаемых в аналитической ГХ, становится все более и более значительным, тогда как коэффициенты емкости колонки быстро увеличиваются. Должны вводиться все меньшие и меньшие пробы, дающие все более и более широкие пики, до тех пор, пока детектирование не станет невозможным. Некоторые преимущества предоставляет уменьшение удельной поверхности используемого сорбента. Оно сокращает продолжительность анализа, но требует использования еще меньших проб. [18]
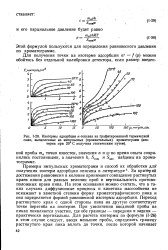 |
Изотермы адсорбции - гексана на графитированной термической саже, вычисленные из импульсных ( проявительных хроматограмм ( изотерма при 20 С получена статическим путем. [19] |
За критерий достижения равновесия в колонне принимают совпадение растянутых краев пиков для разных величин проб и вертикальность противоположных краев пика. На этом основании можно считать, что в таких случаях диффузионные процессы и кинетика массообмена не искажают в заметной степени форму хроматографического пика и она определяется формой равновесной изотермы адсорбции. Переход растянутого края с одной стороны пика на другую соответствует точке перегиба на изотерме. При увеличении вводимой пробы на пиках появляются участки, где обе границы - передняя и задняя - практически вертикальны. [20]
Очевидно, что производная давления по времени сперва возрастает, в средней части остается постоянной и затем падает. Из линейной части зависимости р от - с была определена величина ( др. д) т для каждой температуры. Из равновесных изотерм адсорбции была найдена изостерическая теплота адсорбции. [21]
Экспериментальные факторы, влияющие на адсорбцию. Показано, что равновесные изотермы адсорбции практически не зависят от размера частиц угля марки CaL 12x40, однако имеется зависимость величины адсорбции от рН раствора. [22]
При этом оказалось, что растянутые границы пиков совпадают, а острые почти вертикальны. Поэтому можно считать, что в данном случае диффузионные процессы и кинетика массообмена не искажают в заметной степени форму хроматографического пика. Она определяется формой равновесной изотермы адсорбции. [23]
При замещении около 70 % Са 2 на Na для обоих цеолитов наблюдается своеобразное обращение молекулярно-ситового эффекта при сравнении адсорбции N2, с одной стороны, и С2НБОН и СдН7ОН - с другой. В то же время условия диффузии молекул этилового и пропилового спиртов в полости цеолитов существенно облегчаются, что видно из сопоставления кинетических кривых. При этом для этанола равновесие устанавливается достаточно быстро, поэтому могут быть получены равновесные изотермы адсорбции. [24]
В уравнении хемосорбции (III.2) величина С может меняться от нуля до некоторого предельного значения, соответствующего хемосорбционной емкости концентратора с химическим поглотителем. Предельное значение концентрации хемосорбированных молекул не зависит от концентрации сорбата и меняется не плавно, как в случае физической адсорбции, а скачками. Такое поглощение является необратимым процессом, и здесь фактически нет равновесия, как в случае адсорбции-как бы ни уменьшалась концентрация сорбата С, изменения ( уменьшения) количества поглощенных ( хемосорбированных) молекул не происходит. Графически ( в отличие от равновесной изотермы адсорбции Лэнгмюра) это прямая линия, параллельная оси абсцисс. [25]
Чтобы устранить первую причину размывания хроматографических полос, необходимо выбирать адсорбент, дающий для данных компонентов изотермы адсорбции, возможно близкие к л нейным. Одна из причин успеха газо-жидкостной хроматограф / заключается в линейности изотерм распределения ( адсорбции на гладкой поверхности жидкости [66-68] и растворимости [69]) в широких пределах, перекрывающих область рабочих концентраций. Для легких газов и углеводородов начальные линейные участки изотерм адсорбции получаются и на однороднотонкопористых адсорбентах, на пористых кристаллах. Симметричность пиков на таких адсорбентах указывает на отсутствие размывания, связанного с нелинейностью равновесных изотерм адсорбции компонентов смеси. [26]
Чтобы устранить первую причину размывания хроматографических полос, необходимо выбирать адсорбент, дающий для данных компонентов изотермы адсорбции, возможно близкие к лг нейным. Одна из причин успеха газо-жидкостной хроматограф заключается в линейности изотерм распределения ( адсорбции на гладкой поверхности жидкости [66-68] и растворимости [69]) в широких пределах, перекрывающих область рабочих концентраций. Для легких газов и углеводородов начальные линейные участки изотерм адсорбции получаются и на однороднотонкопористых адсорбентах, на пористых кристаллах. Симметричность пиков на таких адсорбентах указывает на отсутствие размывания, связанного с нелинейностью равновесных изотерм адсорбции компонентов смеси. [27]
Давление газа над адсорбентом соответствует концентрации газа на наружной поверхности адсорбента в соответствии с изотермой адсорбции. При непрерывном поступлении газа эта величина значительно превышает равновесное давление, так как поток газа внутрь адсорбента создает значительное увеличение концентрации адсорбата на поверхности зерна. После прекращения натекания газа давление постепенно уменьшается ( см. рис. 5) вследствие диффузионного выравнивания концентрации адсорбата по сечению зерна. В случае полного выравнивания адсорбции по зерну над адсорбентом достигается минимальное давление, зависимость которого от количества откачанного газа описывается равновесной изотермой адсорбции. [28]
При фронтальной хроматографии концентрация исследуемог вещества в потоке газа-носителя у входа в колонну поддерживается постоянной и регистрируется нарастание его концентрации у выхода из колонны до величины, равной концентрации у входа в колонну. Меняя постоянную концентрацию адсорбата в газе-носителе, получают различные выходные кривые, представляющие зависимости концентрации адсорбата в выходящем из колонны газе от времени выхода. Анализ этих кривых позволяет в благоприятных случаях ( для не слишком медленной адсорбции) получить ряд точек или отрезков для построения изотермы адсорбции. Существенно выбрать оптимальные условия опыта - шаровидную форму, близкие размеры и возможно более однородную упаковку зерен адсорбента ( не содержащих тонких пор), температуру колонны и скорость потока газа, чтобы в наибольшей степени приблизиться к равновесию в колонне и иметь возможность вычислить равновесную изотерму адсорбции из выходных кривых. [29]
Страницы: 1 2