Установление - истинное равновесие
Cтраница 1
Установление истинного равновесия означает полное распределение полимера между равновесными фазами не только по суммарной концентрации, но и по молекулярному весу. Ясно, что такие сложные процессы требуют значительного времени и обусловливают явления гистерезиса. Можно полагать, что к рассмотренной выше картине, связанной с эффектом Ариса, добавляются и тистерезисные явления за счет перераспределения полимера по молекулярному весу между двумя фазами. Уместно рассмотреть в связи с этим вопрос о кривых температур плавления студней. [1]
Добиться установления истинного равновесия оказалось очень трудно, и, несомненно, именно это привело к получению дезориентирующих результатов. Работы Центнершвера по изучению термодинамики указанных систем имеют большое значение, что же касается кинетических исследований, то здесь еще имеется много трудных вопросов. [2]
Но даже и в таких случаях полная уверенность в установлении истинного равновесия достигается иногда лишь при возможности подхода к нему с разных сторон. [3]
Для нас является существенным, в какой мере наличие подобных групп влияет на установление истинного равновесия при изменении состава растворяющей среды. Очевидно, этот процесс, протекающий во времени ( период релаксации системы), будет определяться средним временем жизни подобных групп, и кинетика установления равновесия будет задаваться теми же величинами. Если средний период жизни такой группировки бесконечно велик, то равновесие вообще не установится, и такая группировка будет являться частицей, состав, число и взаимное расположение молекул которой не будут изменяться при изменении состава среды. Таким частицам мы вправе приписать свойства фазы, а всей системе - свойства термодинамически неустойчивого коллоидного раствора. Образование таких агрегатов наиболее возможно в белках. [4]
Трудны для экспериментального изучения и растворы полимеров - здесь в связи с высокой вязкостью жидкой фазы необходимо длительное время установления истинного равновесия. [5]
После достижения точки стеклования система усаживается ( коллапоирует) в результате удаления остаточной воды, но эта усадка не имеет характера установления истинного равновесия, а сопровождается возникновением напряженного состояния макромолекул и их агрегатов. Аналогичную роль может играть и фиксация неравновесного взаимного расположения макромолекул благодаря частичной кристаллизации полимера в процессе сушки. [6]
Как уже отмечено во введении, большое число исследований, посвященных изучению строения поверхности твердых адсорбентов и катализаторов, проводилось без достаточной гарантии установления истинного равновесия между адсорбирующимся веществом и твердым телом. В исследованиях, приведенных в настоящей статье, приняты меры, имевшие целью устранить по возможности этот недостаток. [7]
Тот факт, что разность никогда не равна точно 1 38; объясняется наличием некоторой тенденции к упорядочению структуры, в ре - зультате чего один вид ориентации преобладает над другим В этих случаях энтропия, найденная калориметрическим путем, меньше вычисленной по спектроскопическим данным потому, что при понижении температуры скорость, с которой система переходит к упорядоченному состоянию, очень мала по сравнению со временем, в течение которого длится наблюдение; следовательно, при очень низких температурах наблюдаемые теплоемкости меньше тех, которые соответствовали бы установлению истинного равновесия. Таким образом, величина площади под кривой Ср - In Т, измеряемая при вычислении энтропии, также занижена, и величины, вычисленные по спектроскопическим данным, являются более точными. Расхождение между статистической и калориметрической величинами для энтропии воды, как полагают, связано с координацией молекул Н4О в кристалле посредством водородных связей. [8]
При истинных равновесиях в химических или физических процессах отсутствие видимых изменений и постоянство состава обусловливаются отнюдь не отсутствием взаимодействия. Обязательным условием возможности установления истинного равновесия является возможность течения процессов как в прямом, так и в противоположном направлениях. Равновесие может устанавливаться тогда, когда в системе протекают два процесса, противоположные один другому. Истинное равновесие определяется равенством скоростей этих процессов, в результате чего в единицу времени одинаковое количество вещества претерпевает изменение как в направлении прямого процесса, так и в направлении обратного. [9]
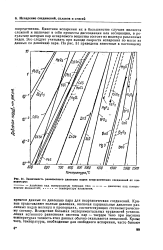 |
Зависимость равновесного давления паров неорганических соединений от температуры. [10] |
Кривые представляют полные давления, включая парциальные давления различных видов молекул в пропорциях, соответствующих стехиометрическо-му составу. Вследствие больших экспериментальных трудностей установления истинного равновесия системы пар - твердое тело при высоких температурах точность этих данных обычно оказывается невысокой. [11]
Процессом, приводящим к установлению истинного равновесия, является процесс длительной перекристаллизации. [12]
Процессом, приводящим к установлению истинного равновесия, является процесс длительной перекристаллизации. С другой стороны, исследования показали, что при некоторых условиях выделения твердой фазы истинное равновесие не устанавливается, и тем самым были объяснены результаты, полученные Дернером и Госкинсом, а также другими авторами. [13]
Экспериментальные исследования, проведенные динамическим методом, дали хорошее совпадение с расчетными данными при адсорбции на Н - эрионите и КОМ. При адсорбции на Н - клиноптилолите и Н - мордените установление истинного равновесия затруднено из-за блокирования входных окон цеолитов большими молекулами четырехокиси и хлорокис-лов азота. [14]
При осаждении гидроокиси магния и карбоната кальция необходимо учитывать их склонность к образованию пересыщенных растворов, особенно характерную для карбоната кальция. В определенных условиях карбонат кальция может образовывать пересыщенные метастабильные растворы, содержащие 200 - 300 мг / л ионов кальция, причем установление истинного равновесия может продолжаться в течение многих часов. Степень пересыщения снижается при повышении температуры, интенсивном перемешивании и внесении затравки. Снятие пересыщения в рассоле происходит значительно медленнее, чем в воде, поэтому очистку рассола проводят в более жестких условиях ( повышенная температура и увеличение избытка реагентов-осадителей), чем при умягчении воды. [15]
Страницы: 1 2