Установление - полное равновесие
Cтраница 2
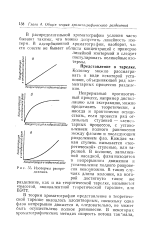 |
Изотермы распределения. [16] |
Непрерывный противоточ-ный процесс, например дистилляцию или экстракцию, можно представить теоретически, а иногда и практически осуществить, если провести ряд отдельных ступеней - элементарных процессов, с установлением полного равновесия между фазами и последующим разделением фаз. Каждая такая ступень называется теоретической ступенью, или тарелкой. В колонке, заполненной насадкой, фазы находятся в непрерывном движении и установление поллого равновесия невозможно. [17]
Эксергия Е - это свойство термодинамической системы или потока энергии, определяемое количеством работы, которое может быть получено внешним приемником энергии при обратимом их взаимодействии с окружающей средой до установления полного равновесия. [18]
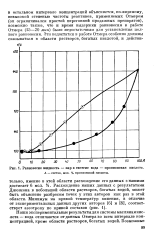 |
Равновесие жидкость - пар в системе вода - пропионовая кислота. А - состав, мол. % пропионовой кислоты. [19] |
Отмером ( он ограничивался простой перегонкой продажных препаратов), возможно также, что и время выдержки равновесия в работе Отмера ( 15 - 20 мин) было недостаточным для установления полного равновесия. [20]
Были построены изотермы адсорбции в области активированной адсорбции, хотя следует иметь в виду, что здесь определение изотермы по методу Глюкауфа носит приблизительный характер, так как нет гарантии установления полного равновесия. [21]
В некотором смысле параметры T ( t) I / / 3 ( t) можно интерпретировать как неравновесные температуры подсистем, поскольку все они стремятся к температуре термостата Т по мере установления полного равновесия в системе. Подчеркнем, однако, что во многих случаях термин неравновесная температура подсистемы не следует понимать буквально. Важным частным случаем распределения (2.2.75) является квазиравновесное распределение для пространственно однородной системы, в которой идут химические реакции. [22]
Поскольку время установления полного равновесия довольно значительное ( 2 - 3 ч; 95 % газа растворяется примерно за 30 мин), наряду с ручной предусмотрена автоматическая подача штока в шприце. Для этой цели на нуль-индикаторе давления установлена оптоэлект-ронная пара фотоэлектрического импульсного, управляющего электродвигателем механизма подачи штока. [23]
Непосредственное практическое использование данных о величинах растворимости также связано с некоторыми затруднениями. В практической аналитической работе химик редко имеет время дожидаться установления полного равновесия. При рапворении иешестви он обыкновенно получает ненасыщенный раствор, л при осаждении - пересышенныи раствор. [24]
Непосредственное практическое использование данных о величинах растворимости также связано с некоторыми затруднениями. В практической аналитической работе химик редко имеет время дожидаться установления полного равновесия. При рапворении нешестви он обыкновенно получает ненасыщевд-шй раствор, л при осаждении - пересышенныи раствор. [25]
В анализаторе Фойра ( рис. VII-7, а) из стеклянной трубки анализируемая газовая смесь подается мембранным насосом через расходомер в рабочую ячейку, снабженную капилляром ртутного капельного электрода [ 2, с. Этим достигается образование равномерной пленки электролита на поверхности капилляра и, следовательно, установление полного равновесия раствор - газовая смесь, а также регулярное образование капель электролита в нижней части капилляра. При этом электролиз реализуется в каждой капле электролита, свободно висящей на конце капилляра, а уровень электролита под капилляром поддерживается строго постоянным, что необходимо для стабилизации процесса каплеобразования, с помощью перелива, соединенного трубкой с сосудом, на дне которого находится постоянный слой ртути, образующий вспомогательный электрод. [26]
В концепции теоретических тарелок развита формальная теория; при этом реальный процесс заменяется идеальным. Разделительная колонка рассматривается в виде некоторой установки, объединяющей ряд элементарных процессов с установлением полного равновесия между фазами и последующим разделением фаз. Каждая такая ступень называется теоретической ступенью или тарелкой. [27]
Можно ожидать, что не только параметр порядка ф, но и плотность энергии е медленно релаксируют. Однако поскольку соответствующая восприимчивость С гораздо меньше х, то энергия сравнительно быстро приходит в равновесие при заданном ф, и время установления полного равновесия определяется параметром порядка. [28]
Температура неравновесной смеси продуктов сгорания значительно превышает Ть. За пределами зоны взаимодействия Н2 С12 сравнительно медленная диссоциация избыточного хлора не прекращается, она продолжается в продуктах сгорания и завершается с установлением полного равновесия на достаточном удалении от зоны интенсивной реакции. Так как диссоциация хлора - процесс эндотермический, по мере образования атомарного хлора температура будет понижаться. В зоне реакции возникает максимум температуры. Взаимодействие между Н2 С12 протекает при концентрации активных центров значительно меньшей равновесной и соответственно более высокой температуре. Атомы хлора в основном генерируются за пределами зоны реакции и переносятся в эту зону диффузией. [29]
Температура неравновесной смеси продуктов сгорания значительно превышает Ть. За пределами зоны взаимодействия Н2 С12 сравнительно медленная диссоциация избыточного хлора не прекращается, она продолжается в продуктах сгорания и завершается с установлением полного равновесия на достаточном удалении от зоны интенсивной реакции. Так как диссоциация хлора - процесс эндотермический, по мере образования атомарного хлора температура будет понижаться. В зоне реакции возникает максимум температуры. Взаимодействие между Н2 СЬ протекает при концентрации активных центров значительно меньшей равновесной и соответственно более высокой температуре. Атомы хлора в основном генерируются за пределами зоны реакции и переносятся в эту зону диффузией. [30]
Страницы: 1 2 3 4