Установление - полное равновесие
Cтраница 3
Температура неравновесной смеси продуктов сгорания значительно превышает Ть. За пределами зоны взаимодействия Н2 С12 сравнительно медленная диссоциация избыточного хлора не прекращается, она продолжается в продуктах сгорания и завершается с установлением полного равновесия на достаточном удалении от зоны интенсивной реакции. Так как диссоциация хлора - процесс эндотермический, по мере образования атомарного хлора температура будет понижаться. В зоне реакции возникает максимум температуры. Взаимодействие между Н2 С12 протекает при концентрации активных центров значительно меньшей равновесной и соответственно более высокой температуре. Атомы хлора в основном генерируются за пределами зоны реакции и переносятся в эту зону диффузией. [31]
Для тройной металлической системы, так же как и для двойной, речь может идти о равновесии жидкое-твердое - результатом является построение изотерм и поверхности солидуса - или же о равновесии в твердокристал-лическом состоянии - об изотермах растворимости в металлах или их соединениях в твердом состоянии. Она заключается, как и при построении двойных систем, в изучении фазового состава образцов сплава после длительного отжига при заданной температуре до установления полного равновесия и фиксировании этого равновесия закалкой - быстрым охлаждением в область температуры ниже той, при которой возможна диффузия в сплаве. [32]
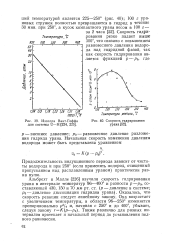 |
Изохора ВантТоффа для системы U - Н.| Скорость гидрирования урана. [33] |
Оказалось, что скорость реакции следует линейному закону. Она возрастает с увеличением температуры, в области 96 - 250 изменяется пропорционально р3Д я, начиная с - 250 и до 400, убывает, следуя закону г - К ( р - ро) Также различно для разных интервалов протекает и начальный период до установления полного равновесия. [34]
 |
Жидкостная граница в проточной системе. [35] |
Через межэлектролитные границы возможна диффузия всех ионов, которые могут существовать в обеих фазах. Диффузия приводит к выравниванию электрохимического потенциала ионов и в итоге - к установлению равновесного распределения между фазами. Процесс установления полного равновесия, как правило, длителен. Поэтому для таких систем рассматривают только явления в заданном исходном состоянии, до наступления равновесия ( разд. [36]
При этом она описывает состояние полного статистического равновесия системы. По структуре такая функция совпадает с квазиравновесной функцией (8.3), в которой роль Ат играют аддитивные интегралы движения - энергия HN и число частиц N. Если состояние термостата меняется со скоростью, много меньшей скорости установления полного равновесия в системе, то система, оставаясь в полном равновесии, будет постепенно переходить из одного равновесного состояния в другое. Иными словами, параметры равновесного распределения - средняя энергия и среднее число частиц - будут плавно меняться во времени вслед за изменением параметров термостата. Такое изменение равновесного состояния системы называют квазистатическим процессом. Строго говоря, для его осуществления требуется бесконечно медленное изменение внешних условий. Поскольку состояние системы, участвующей в квазистатическом процессе, определяется на каждом интервале времени внешними условиями на том же интервале, то, меняя условия в обратном порядке, повторим в обратном порядке и квазистатический процесс. Это значит, что квазистатический процесс обратим. [37]
Ячейка с ртутным индикаторным электродом ( рис. 5, а) снабжена капиллярным ртутным капельным электродом 1, установленным в сосуде 2, содержащем электролит ( раствор соляной кислоты), поступающий в сосуд из специальной емкости. Ртуть в капиллярный электрод поступает из емкости, в которой она хранится. Выдыхаемый воздух подается в ячейку навстречу движущемуся вдоль капельного электрода электролиту, что обеспечивает образование равномерной пленки электролита на поверхности капилляра и установление полного равновесия раствор - газовая смесь, а также систематическое образование капель электролита в нижней части капилляра. [38]
Наиболее ярко неравновесное распределение вращательной энергии, выделяющейся в экзотермических реакциях, проявляется в спектре пламени. Энергия, освобождающаяся в ходе экзотермической реакции, часто принимает форму лучистой энергии, поэтому такая реакция сопровождается излучением света - пламенем. Обычно в зоне реакции пламен, горящих при предварительном перемешивании горючего с воздухом или кислородом, интенсивность излучения некоторых радикалов, особенно ОН, СО2 и СН2, значительно превышает величину, которую можно было бы ожидать при установлении полного равновесия в зоне горения. [39]
Так как состав сосуществующей жидкой фазы отличается от состава молекулярного соединения, то говорят об инкогруэнтной температуре плавления соединения. Соответствующий этой температуре гипотетический максимум должен был бы находиться в точке М на продолженном пунктиром отрезке кривой EL, характеризующем метастабильное состояние. Все смеси, состав которых лежит между токами L и В, после первичной кристаллизации компонента В при температурах, соответствующий кривой LB, обогащаются кристаллическим компонентом В, вплоть до температуры, соответствующей точке превращения. При условии медленного охлаждения и установления полного равновесия между фазами происходит последующее выделение молекулярного соединения АтВп, образующегося при взаимодействии жидкой фазы и уже выкристаллизовавшегося компонента В. В этой области сосуществуют две твердые и одна жидкая фазы, и конденсированная система становится инвариантной. Кристаллизация всех этих смесей происходит при одной и той же постоянной температуре до тех пор, пока твердая фаза компонента В полностью не перейдет в молекулярное соединение или же пока жидкая фаза полностью не затвердеет. Последний процесс происходит при всех составах смесей, которые содержат больше компонента В, чем это требуется по составу молекулярного соединения. В противоположность этому для смесей, содержащих меньше компонента В, чем его содержится в молекулярном соединении ( интервал LM), происходит полный переход твердой фазы компонента В в молекулярное соединение и кристаллизуется только молекулярное соединение, а остающаяся жидкость обогащается компонентом В. При дальнейшем охлаждении из жидкости вновь выделяется некоторое количество молекулярного соединения, пока оно не затвердеет совместно с компонентом А при эвтектической температуре. При расплавлении твердой смеси компонентов протекают эти же процессы, но в обратном порядке. [40]
Так как состав сосуществующей жидкой фазы отличается от состава молекулярного соединения, то говорят об инкогруэнтной температуре плавления соединения. Соответствующий этой температуре гипотетический максимум должен был бы находиться в точке М на продолженном пунктиром отрезке кривой EL, характеризующем метастабильное состояние. Все смеси, состав которых лежит между токами L и В, после первичной кристаллизации компонента В при температурах, соответствующих кривой LB, обогащаются кристаллическим компонентом В, вплоть до температуры, соответствующей точке превращения. При условии медленного охлаждения и установления полного равновесия между фазами происходит последующее выделение молекулярного соединения А, В, образующегося при взаимодействии жидкой фазы и уже выкристаллизовавшегося компонента В. В этой области сосуществуют две твердые и одна жидкая фазы, и конденсированная система становится инвариантной. Кристаллизация всех этих смесей происходит при одной и той же постоянной температуре до тех пор, пока твердая фаза компонента В полностью не перейдет в молекулярное соединение или же пока жидкая фаза полностью не затвердеет. Последний процесс происходит при всех составах смесей, которые содержат больше компонента В, чем это требуется по составу молекулярного соединения. В противоположность этому для смесей, содержащих меньше компонента В, чем его содержится в молекулярном соединении ( интервал LM), происходит полный переход твердой фазы компонента В в молекулярное соединение и кристаллизуется только молекулярное соединение, а остающаяся жидкость обогащается компонентом В. При дальнейшем охлаждении из жидкости вновь выделяется некоторое количество молекулярного соединения, пока оно не затвердеет совместно с компонентом А при эвтектической температуре. При расплавлении твердой смеси компонентов протекают эти же процессы, но в обратном порядке. [41]
А в парах будет ниже, а в жидкости выше, чем должно быть в состоянии равновесия. Однако пары, не успев дойти до такого состояния, проникают на первую тарелку, где наблюдается то же явление. На вторую тарелку пары попадают не только до установления полного равновесия, но даже и до того максимального к нему приближения, которое осуществимо при данной конструкции тарелки ( см. стр. Так, продвигаясь преждевременно с тарелки на тарелку, пары доходят, наконец, и до верхней тарелки, а оттуда попадают в приемник. [42]
Материалы, приведенные в предыдущих главах, свидетельствуют о том, что наиболее правильным подходом к объяснению разнообразных явлений взаимодействия воды с целлюлозой служит представление о подчиняе-мости этой системы тем закономерностям, которые характерны вообще для любой системы полимер - низкомолекулярная жидкость. Если полимер закристаллизован, то взаимодействие с низкомолекулярной жидкостью ( ее парами) происходит лишь на поверхности кристаллитов. При этом, естественно, имеется в виду тот случай, когда низ. Первичным актом здесь является, вероятно, сорбция на поверхности, но далее происходит установление полного равновесия, при котором молекулы низкомолекулярного вещества оказываются равномерно распределенными во всем объеме аморфного полимера. [43]
С повышением температуры, все более нарушается равновесное распределение энергии по внутренним степеням свободы частиц в процессе их диссоциации. Скорость химической реакции в неравновесных условиях, вообще говоря, зависит от эффективных сечений многих элементарных процессов. Имеются, однако, случаи, когда даже при сильном нарушении равновесия возможно описание кинетики реакции на основе представлений о равновесной константе скорости. Это удается сделать, если в системе есть быстрые процессы, которые, хотя и не ведут к установлениях полного равновесия, но обеспечивают равновесие внутри подсистемы. Тогда неравновесность выражается лишь в том, что система характеризуется не одной, а двумя или несколькими температурами. [44]
Мы уже видели, что наличие такого катализатора, как пары воды, способствует установлению теплового равновесия за счет дезактивации молекул с возбужденными колебаниями при столкновениях. Поэтому следует ожидать, что рассмотренное выше увеличение степени диссоциации будет меньше при горении в присутствии влаги или водорода. Так, для обычных топлив эффект увеличения степени диссоциации гораздо менее заметен. При определении степени диссоциации следует помнить, что химический анализ продуктов горения вряд ли может показать истинный состав смеси в тот момент, когда выхлопные газы покидают двигатель, поскольку степень диссоциации будет уменьшаться в течение накопления пробы за счет установления полного равновесия. [45]
Страницы: 1 2 3 4