Установление - первичная структура
Cтраница 1
Установление первичной структуры пептида или белка дает возможность получить соединение синтетическим путем. Совокупность синтетических операций, приводящих к получению пептидов из аминокислот, называется пептидным синтезом и как и всякий другой раздел органического синтеза отличается особенностями, присущими синтезу только этого типа соединений. Грубая схема объединения двух аминокислот в дипептид ( аминокислота 1 аминокислота 2 - дипептид) не отражает тех проблем, которые необходимо решить при создании пептидной молекулы. [1]
Установление первичной структуры 55 РНК из Esche-richia coll: Al - продукт частичного гидролиза гуанил - РНК-азой: Б1, Б2 - продукты частичного гидролиза пиримидил - РНК-азой; В1 - продукт частичного гидролиза кислой РНК-азой селезенки; П, Г2 - продукты гидролиза гуанил - РНК-азой после предварительного метилирования; Д1 - продукт гидролиза пири-мидил - РНК-азой после обработки карбодиимидом; El, E2 - продукты полного гидролиза гуанил - РНК-азой; Ж1, Ж2 - продукты полного гидролиза пиримидил - РНК-азой. [2]
Установление первичной структуры пептида или белка дает возможность получить соединение синтетическим путем. Совокупность синтетических операций, приводящих к получению пептидов из аминокислот, называется пептидным синтезом и как и всякий другой раздел органического синтеза отличается особенностями, присущими синтезу только этого типа соединений. Грубая схема объединения двух аминокислот в дипептид ( аминокислота 1 аминокислота 2 - дипептад) не отражает тех проблем, которые необходимо решить при создании пептидной молекулы. [3]
Установление первичной структуры начинается с определения аминокислотного состава и молекулярной массы выделенного и очищенного белка. Белки, состоящие из нескольких полипептидных цепей, разделяются с помощью денатурирующих реагентов ( концентрированный раствор мочевины или ДСН) на мономеры. Дисульфидные мостики расщепляют восстановлением меркаптоэтанолом. Для предотвращения дисульфидного обмена и окисления образующихся свободных меркаптогрупп их блокируют каким-либо методом, например алкилированием иодуксусной кислотой с образованием S-карбоксиметильного производного или цианэтилированием акри-лонитрилом. После определения N - и С-концевых аминокислот полипептидная цепь расщепляется химически или ферментативно ( в нескольких вариантах) на меньшие перекрывающиеся фрагменты. Для каждого фрагмента устанавливается аминокислотная последовательность. И наконец, комбинируя отдельные последовательности, приходят к полной последовательности исходной полипептидной цепи. [4]
 |
Структура клеверного листа фенилаланиновой тРНК. [5] |
Установление первичной структуры большого числа транспортных РНК показало, что все они построены таким образом, что у них имеется три пары комплементарных фрагментов, разделенных участками в несколько нуклеотидных остатков, не имеющих партнеров для образования сколько-нибудь протяженных комплементарных участков. [6]
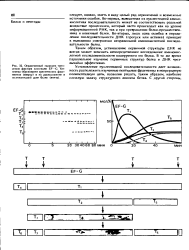 |
Ограниченный гидролиз трипсином фактора элонгации EF-G. Кинетика образования трнптических фрагментов ( вверху и их расположение в полипептидной цепи белка ( внизу. [7] |
Таким образом, установление первичной структуры ДНК не всегда может заменить непосредственное исследование аминокислотной последовательности кодируемого ею белка. В то же время параллельное изучение первичных структур белка и ДНК чрезвычайно эффективно. [8]
Очень интересные возможности установления первичной структуры углеводсодержащих биополимеров открывает принцип индуцирования экзоферментов, который был предложен в работах Стейси и Баркера. Если этот принцип окажется достаточно универсальным, а его аналитическое оформление будет хорошо разработано, он может оказаться очень полезным для анализа концевых последовательностей в полисахаридных цепях. [9]
В последнее время проблема установления первичной структуры ферментов и других белков развивается весьма успешно. [10]
Число лабораторий, занимающихся установлением первичной структуры нуклеиновых кислот, быстро растет. В свою очередь эти достижения были бы невозможны без создания целого ряда высокочувствительных и надежных методик. Для многих исследователей работа по выяснению структуры нуклеиновых кислот является лишь частью другой проблемы, например синтеза или биохимической эволюции белков и нуклеиновых кислот. [11]
 |
Жидкостной микроколоночный хроматограф ХЖ-1311 с флуоресцентным детектором ( НТО А Н ССС Р, г Ленинград. [12] |
Наиболее широко используемым ферментом при установлении первичной структуры белков является трипсин. Коммерческий бычий трипсин получают активацией его предшественника трипсиногена, выделяемого из секрета поджелудочной железы. [13]
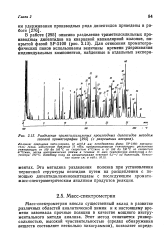 |
Разделение триметилсилильных производных дипептидов методом газовой хроматографии ( с разрешения авторов. [14] |
Эта методика разделения полезна при установлении первичной структуры пептидов путем их расщепления с помощью дипептидилам инопептидазы с последующим хромато масс-спектрометрическим анализом продуктов реакции. [15]
Страницы: 1 2 3