Медленное установление - равновесие
Cтраница 2
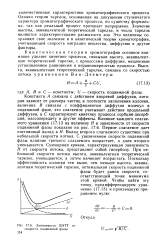 |
Зависимость ВЭТТ от. [16] |
Кинетическая теория хроматографии основное внимание уделяет кинетике процесса, связывая высоту, эквивалентную теоретической тарелке, с процессами диффузии, медленным установлением равновесия и неравномерностью процесса. [17]
Практическая важность вопроса связана прежде всего с тем, что во многих экстракционных системах равновесие достигается отнюдь не мгновенно; примеры медленного установления равновесия будут приведены ниже. Кроме того, факты показывают, что время достижения равновесия зависит от условий проведения экстракции. Теоретический интерес к кинетике обусловлен возможностью получения полезной информации о механизме экстракционного процесса. [18]
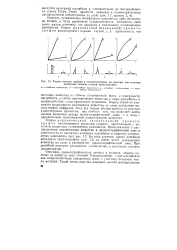 |
Формы изотерм сорбции и соответствующие им контуры зон согласно различным теориям газовой хроматографии. [19] |
Скорость установления межфазного равновесия либо бесконечно велика, и тогда равновесие устанавливается мгновенно, либо имеет малую величину, что приводит к медленному установлению равновесия. [20]
В монокарбоновых кислотах ( муравьиная, уксусная, хлоруксусная, глицин, молочная и миндальная) наблюдается образование платиновыми металлами широких зон из-за медленного установления равновесия между различными комплексными формами, поэтому такие кислоты для разделений не пригодны. [21]
Хотя в зависимости от свойств определенной экстракционной системы процессом, определяющим кинетику экстракции, может стать как первая, так и вторая стадии, в большинстве случаев медленное установление равновесия определяется, по-видимому, химическими реакциями в водной и органической фазах. [22]
Хотя в зависимости от свойств определенной экстракционной системы процессом, определяющим кинетику экстракции, может стать как первая, так и вторая стадия, в большинстве случаев медленное установление равновесия определяется химическими реакциями в водной и органической фазах. [23]
Одной из причин возникновения продолговатых пятен, занимающих область в несколько десятых Я (, может быть медленное установление сорбционного равновесия между неподвижной и подвижной фазами или медленное установление равновесия между двумя формами одного и того же вещества в растворе по сравнению с быстрым движением растворителя ( см. стр. Однако продолговатые пятна могут быть обусловлены и другими причинами. Ниже мы рассмотрим некоторые особые случаи. [24]
Таким образом, подводя итог, можно сказать, что в тех случаях, когда образуются биконтинуальные структуры, не следует удивляться экспериментально обнаруженным энтропийным явлениям, например медленному установлению равновесия, гистерезису в фазовых переходах и наличию метастабильных равновесных состояний или полиморфизму. [25]
Сложная система уран - кислород была предметом многих исследований [1, 2], в которых были получены противоречивые результаты из-за образования твердых растворов переменного состава между разными модификациями нескольких окислов и медленного установления равновесия между компонентами твердых фаз и кислородом. Кроме них давно известна перекись состава U04 2Н20 и недавно обнаружена вторая перекись U20, [3], существование которой подтверждено термическим разложением первой [4], а также в настоящей работе. О строении U04 2Н20 представления до сих пор остаются противоречивыми. [26]
Широко известные ( 3-дикетоны - ацетилацетон, дибензоилметан, теноил-трифторацетон - мало удобны, первый - из-за высокой растворимости в воде и слабой экстракционной способности ( многие элементы вообще не экстрагируются, другие извлекаются с малыми коэффициентами распределения или при относительно высоких рН), второй - из-за медленного установления равновесия, третий - вследствие сложности синтеза, малой доступности, неустойчивости при хранении и трудности очистки. [27]
Это медленное установление равновесия имеет большое физиологическое значение и очень важно в биологической, аналитической и промышленной химии. Эту реакцию можно наглядно показать добавлением насыщенного водного раствора СО. [28]
 |
Кривые экстракции. [29] |
Однако при экстракции внутрикомплексных соединений скорость установления равновесия может быть низкой, особенно при малых концентрациях реагентов. Случаи медленного установления равновесия известны для систем с такими хелатообразующи-ми реагентами, как дитизон, теноилтрифторацетон, ацетилацетон. Скорость экстракции снижается также в присутствии в водной фазе маскирующих агентов. Поэтому при разработке новой экстракционной методики важно учитывать не только равновесные, но и кинетические характеристики системы. [30]
Страницы: 1 2 3 4