Медленное установление - равновесие
Cтраница 3
При небольшом избытке лигандных групп в системе определяющей является скорость изменения конформа-ционного набора полимера для образования координационных центров, обусловленных электронной конфигурацией ионов металла-комплексообразователя. Из-за чрезвычайно медленного установления равновесия изучать кинетику процесса комплексообразования в этих системах весьма сложно. Поэтому экспериментальное определение скорости сорбции ионов переходных металлов комплексообразующими ионитами большинство исследователей проводили в условиях большого избытка лигандных групп, что обеспечивает диффузионную кинетику процесса. Однако кинетику реакции комплексообразования в этих условиях определить не удается. [31]
Если растворы не содержат окислителей или ядов специфического действия, то в практике измерений рН водородный электрод является очень полезным. Его основными недостатками являются медленное установление равновесия и необходимость применять большой объем исследуемого раствора. [32]
Если растворы не содержат окислителей, или ядов специфического действия, то в практике измерений рН водородный электрод является очень полезным. Его основными недостатками являются медленное установление равновесия и необходимость применять большой объем исследуемого раствора. [33]
 |
Сурьмяный электрод. [34] |
Водородный электрод обладает хорошей воспроизводимостью при соблюдении многих условий, в особенности: чистоты электролита, водорода, высокой степени чистоты поверхности электрода, стандартной величины пузырьков водорода и глубины их погружения. Основными недостатками водородного электрода являются медленное установление равновесия и необходимость применять большой объем исследуемого раствора. [35]
Возможность и необходимость изменения порядка титрования в известной мере определяется скоростью титрования. Иногда титрование оказывается невозможным из-за медленного установления равновесия. В этом случае приходится изменять способ титрования. Например, прямое титрование свинца и цинка раствором ЭДТА в присутствии дитизона малоудобно, ибо реакция проходит медленно. [36]
На вязкость так же, как и на осмотическое давление достаточно концентрированных растворов высокомолекулярных веществ, может влиять способ приготовления раствора. И здесь такое влияние объясняется медленным установлением равновесия в системе. Наконец, на вязкость растворов высокомолекулярных веществ может влиять введение в раствор небольших количеств некоторых веществ. Из практики, например, известно, что вязкость растворов эфиров целлюлозы при введении все возрастающих количеств спирта сначала падает, а затем возрастает. Подобные же явления наблюдаются л при введении в. [38]
 |
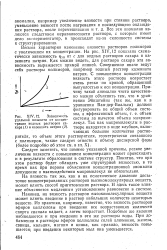
Зависимость удельной вязкости от концентрации водных растворов сахара ( / и казеината натрия ( 2. [39] |
На вязкость так же, как и на осмотическое давление достаточно концентрированных растворов высокомолекулярных веществ, может влиять способ приготовления раствора. И здесь такое влияние объясняется медленным установлением равновесия в системе. Наконец, на вязкость растворов высокомолекулярных веществ может влиять введение в раствор небольших количеств некоторых веществ. Из практики, например, известно, что вязкость растворов эфиров целлюлозы при введении все возрастающих количеств спирта сначала падает, а затем возрастает. Подобные же явления наблюдаются и при введении в эти же растворы воды. [40]
Из приведенных результатов видно, что вычисленные / С во всех случаях больше найденных экспериментально. Это не является случайностью и объясняется тем, что из-за медленного установления равновесия в твердой фазе, кристаллизующиеся твердые растворы обогащены компонентом, играющим роль растворителя. [41]
Оно сводится к исследованию растворимости. Для систем типа расплав - твердое тело часто возникают некоторые затруднения, связанные с медленным установлением равновесия в твердой фазе, а также сложностью полного отделения от нее жидкой фазы. [42]
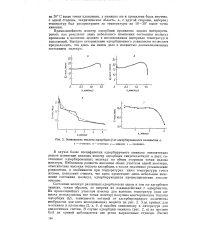 |
Зависимость теплоты адсорбции Q от адсорбированного количества а. а - м-гекоан. 6 - к-гептан. в - аммиак. г - пропилен. [43] |
В случае более специфически адсорбируемого аммиака относительно резкое изменение наклона изостер адсорбции свидетельствует о двух состояниях адсорбированных молекул по обеим сторонам точки излома изостеры. Небольшая разность наклонов обоих участков одной изостеры, относительно высокая теплота адсорбции, а также медленное установление равновесия, в особенности при температурах ниже температуры точки излома, позволяют считать, что здесь происходит лишь небольшое изменение состояния молекул, адсорбирующихся преимущественно локали-зованно. [44]
Подобное явление наблюдается в случае некоторых жидкостей, которые ниже температуры плавления переходят не в кристаллическое состояние, а в стеклообразное, имеющее энтропию большую нуля вблизи О К. Хотя стеклообразное состояние характеризуется более высокой энергией Гиббса, оно не превращается в кристаллическое из-за медленного установления равновесия при низких температурах. Таким образом, отличие от нуля калориметрически измеряемой энтропии замороженных тел не противоречит третьему закону, а обусловлено тем, что они не находятся в состоянии термодинамического равновесия. [45]
Страницы: 1 2 3 4