Устойчивость - дисперсия
Cтраница 2
Более рациональным способом является повышение устойчивости дисперсий к замораживанию путем изменения свойств полимерных частиц. Для этого при сополимеризации применяют15 дополнительные гидрофилизирующие мономеры-ненасыщенные кислоты ( акриловую, метакриловую, малеи-новую) и их соли, растворимые в воде. Таким путем получают вполне морозоустойчивые дисперсии, не коагулирующие при многократном длительном замораживании до - 70 и выдерживающие хранение в зимних условиях. [16]
Из приведенных данных по исследованию устойчивости дисперсии алмаза в растворах КС1 следует, что в зависимости от рН дисперсионной среды и концентрации электролита и, как следствие этого, от состояния поверхности дисперсия алмаза ведет себя либо как лиофилизованная ( кислая область), либо как ионно-стабилизированная ( щелочная область) дисперсная система, обнаруживая тем самым различную чувствительность к добавлению индифферентного электролита. В зависимости от состояния поверхности частиц алмаза ( соотношения числа диссоциированных и недиссоциированных поверхностных групп), возможности образования водородных связей между молекулами воды и поверхностными группами алмаза, а также от концентрации добавленного электролита меняется структура воды в ГС, и, как следствие, соотношение между молекулярной, ионно-электростатической и структурной составляющими энергии взаимодействия частиц. [17]
Ниже будут рассмотрены основы теории устойчивости лиофоб-ных дисперсий, без знания которых невозможно их правильное техническое использование. [18]
Однако верхний предел концентрации ограничен фактором устойчивости дисперсии, ее вязкостью, а также характером и количеством полимера-загустителя и методом его введения. [19]
Подпитка газом из окружающей жидкости обеспечивает их устойчивость относительно капиллярной дисперсии или, по крайней мере, быстрое восстановление связности. Это приводит к увеличению фильтрационного сопротивления для жидкой фазы и соответствующему снижению ее расхода. [20]
Все приведенные выше данные о температурной зависимости устойчивости дисперсии ПА свидетельствуют о том, что повышение температуры при постоянной концентрации электролита приводит к частичному разрушению и утончению ГС. При этом появляется возможность сближения частиц, реализации более глубокого энергетического минимума и, следовательно, роста степени агрегации. Тип и концентрация электролита, как обсуждалось выше, в известной мере определяют структуру и протяженность ГС и, следовательно, оказывают влияние на характер изменения степени агрегации частиц ПА с ростом температуры. [21]
Молекулярно-адсорбционная стабилизация дисперсных систем играет большую роль в устойчивости дисперсий как в водной, так и в неводных средах. [22]
Молекулярно-адсорбционная стабилизация дисперсных систем играет большую роль в устойчивости дисперсий как в водной, так и в неводных средах. Дисперсные системы в неводных средах в принципе менее устойчивы, чем в водной среде. В неполярной и не содержащей воды дисперсионной среде частицы дисперсной фазы лишены электрического заряда. Электрический фактор стабилизации отсутствует. [23]
Молекулярно-адсорбционная стабилизация дисперсных систем играет большую роль в устойчивости дисперсий как в водной, так и в неводных средах. Дисперсные системы в неводных средах в принципе менее устойчивы, чем в водной среде. [24]
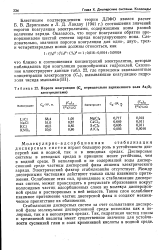 |
Пороги коагуляции ( Ск отрицательно заряженного золя электролитами. [25] |
Молекулярно-адсорбционная стабилизация дисперсных систем играет большую роль в устойчивости дисперсий как в водной, так и в неводных средах. Дисперсные системы в неводных средах в принципе менее устойчивы, чем в водной среде. В неполярной и не содержащей воды дисперсионной среде частицы дисперсной фазы лишены электрического заряда. Электрический фактор стабилизации отсутствует. Между дисперсными частицами действуют только силы взаимного притяжения. Ослабление этих сил, приводящее к стабилизации дисперсных систем, может происходить в результате образования вокруг коллоидных частиц адсорбционных слоев из молекул дисперсионной среды и растворенных в ней веществ. Такие слои ослабляют нзаимное притяжение частиц дисперсной фазы и создают механическое препятствие их сближению. [26]
Молекулярно-адсорбционная стабилизация дисперсных систем играет большую роль в устойчивости дисперсий как в водной, так и в неводных средах. Дисперсные системы в неводных средах в принципе менее устойчивы, чем в водной среде. В неполярной и не содержащей воды дисперсионной среде частицы дисперсной фазы лишены электрического заряда. Электрический фактор стабилизации отсутствует. Между дисперсными частицами действуют только силы взаимного притяжения. Ослабление этих сил, приводящее к стабилизации дисперсных систем, может происходить в результате образования вокруг коллоидных частиц адсорбционных слоев из молекул дисперсионнной среды и растворенных в ней веществ. Такие слои ослабляют взаимное притяжение частиц дисперсной фазы и создают механическое препятствие их сближению. [27]
Молекулярно-адсорбционная стабилизация дисперсных систем играет большую роль в устойчивости дисперсий как в водной, так и в неводных средах. Дисперсные системы в неводных средах в принципе менее устойчивы, чем в водной среде. [28]
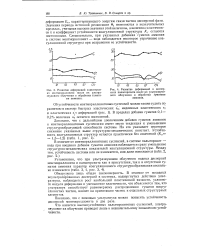 |
Развитие деформаций вдисперси - [ IMAGE ] Развитие деформаций в диспер. [29] |
Показано, что с помощью ультразвука можно повысить устойчивость дисперсий монтмориллонита в два раза. [30]
Страницы: 1 2 3 4