Устойчивость - лиофобные золи
Cтраница 1
Устойчивость лиофобных золей значительно повышается, если на поверхности частиц вместо ионных адсорбционных слоев образуются молекулярные адсорбционные слои за счет адсорбции поверхностно-активных веществ или высокомолекулярных веществ при добавлении их к золю в небольших количествах. При этом поверхность становится гидрофильной и частицы приобретают стабильность. Это явление называется защитой. Примером такого защищенного золя может служить коларгол, золь серебра, защищенный солями лизальбиновой и протальби-новой кислот, который продается в виде сухого порошка, растворимого в воде. Защитное действие проявляется в следующем: 1) золи становятся более устойчивыми к добавкам электролитов; 2) могут быть получены в более высоких концентрациях; 3) их можно обратимо коагулировать и этим путем еще больше повысить концентрацию; 4) можно получить их в виде сухих препаратов, растворимых в дисперсионной среде. В качестве защитных коллоидов применяется желатина, казеин, другие белки, агар, крахмал, декстрин, таннин, полисахариды. Защитное действие зависит от природы защитного коллоида и лиофобного золя и характеризуется золотым числом. Золотое число - это минимальное число миллиграммов сухого вещества, достаточное для предотвращения перемены окраски из красной в синюю 10 мл гидрозоля золота ( 0 05 - 0 06 г золота на л) при добавлении к нему 1 мл 10 % раствора хлористого натрия. [1]
Описание устойчивости лиофобных золей включает обстоятельное рассмотрение теории кинетики быстрой коагуляции по Смолу-ховскому, приближенное изложение теории устойчивости и коагуляции электролитами Дерягина-Ландау - Фервея-Овербека. При описании структуры пен особое внимание уделяется роли черных пленок, образующихся при определенных, критических концентрациях поверхностно-активных веществ. Здесь болгарским ученым также принадлежит ведущая роль. [2]
В теории устойчивости лиофобных золей, развитой Дерягиным, Ландау, Фервеем и Овербеком, предполагается, что диффузная часть двойного электрического слоя ( ДЭС), возникающего у поверхности коллоидных частиц в растворах электролитов, простирается до самой границы раздела фаз. Такое предположение допускает наиболее простую математическую трактовку. На самом деле, однако, непосредственно у поверхности частиц золя расположен так называемый молекулярный конденсатор ( штерновский слой); диффузная же часть ДЭС начинается лишь за внешней обкладкой этого конденсатора, находящейся на расстоянии 3 - 6 А от границы раздела фаз. [3]
Успешное развитие теории устойчивости лиофобных золей служит доказательством того, что в таких системах единственная существенная особенность строения граничного слоя определяется присутствием ионных атмосфер. Все это, однако, относится строго только к лиофобным системам. [4]
Количественные соотношения, характеризующие устойчивость лиофобных золей, в удовлетворительном согласии с экспериментом были получены на основе физической теории устойчивости, развитию которой способствовали работы Б. В. Дерягина и его школы. [5]
 |
Потенциальные кривые ЛЯЦИИ. [6] |
Количественные соотношения, характеризующие устойчивость лиофобных золей, в удовлетворительном согласии с экспериментом были получены на основе физической теории устойчивости, развитию которой способствовали работы Б. В. Дерягина и его школы. Поведение коллоидных систем определяется в соответствии с этой теорией соотношением сил взаимного притяжения и отталкивания частиц. [7]
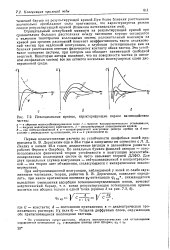 |
Потенциальные кривые, характеризующие парное взаимодействие частиц. [8] |
Первые количественные расчеты по устойчивости лиофобных золей произведены Б. В. Дерягиным еще в 30 - е годы и завершены им совместно с Л. Д. Ландау в начале 40 - х годов; аналогичные взгляды в дальнейшем развиты в работах Фервея и Овербека. По начальным буквам фамилий авторов - основоположников физической теории устойчивости и коагуляции ионностаби-лизированных коллоидных систем ее часто называют теорией ДЛФО. Для двух предельных случаев коагуляции - нейтрализационной и концентрационной - эта теория дает объяснения, согласующиеся с эмпирическими закономерностями. [9]
Рассмотренные выше представления об устойчивости лиофобных золей носят чисто качественный характер. Дерягин и Ландау 13, пользуясь теорией сильных электролитов Дебая-Гюккеля, рассмотрели этот вопрос с количественной стороны и построили математическую теорию устойчивости лиофобных систем. [10]
Рассмотренные выше представления об устойчивости лиофобных золей носят чисто качественный характер. Дерягин и Ландау 13, пользуясь теорией сильных электролитов Дебая-Гюккеля, рассмотрели этот вопрос с количественной стороны и построили математическую теорию устойчивости лиофобных систем. [11]
 |
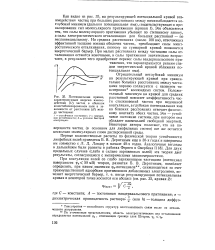
Зависимость отношения порогов коагуляции от. [12] |
Проведен общий анализ критерия устойчивости концентрированных лиофобных золей и на его основе сделаны качественные заключения о влиянии содержания дисперсной фазы на закономерности коагуляции смесями электролитов. [13]
 |
Потенциальные кривые, характеризующие энергию взаимодействия ( U частиц в обычном ионостабилизированном золе в зависимости от расстояния ( Н между частицами. [14] |
Первые количественные расчеты по физической теории устойчивости лиофобных золей приведены Б. В. Дерягиным еще в 30 - х годах и завершены им совместно с Л. Д. Ландау в начале 40 - х годов. Для двух предельных случаев ( слабо и сильно заряженных золей) эта теория дает результаты, согласующиеся с эмпирическими закономерностями. [15]
Страницы: 1 2