Устойчивость - комплексный ион
Cтраница 1
 |
Мо юкуллрнап электропроводность К. с. [1] |
Устойчивость комплексного иона в растворе зависит от свойств центрального иона - от его заряда, размера и электронной структуры. Как правило, чем выше заряд центрального иона, тем устойчивее ионные К. [2]
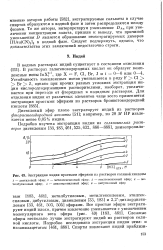 |
Экстракция индия простыми эфирами из растворов соляной кислоты. [3] |
Устойчивость комплексных ионов уменьшается в ряду F С1 Вг J, однако при прочих равных условиях экстракция индия - кислородсодержащими растворителями, наоборот, увеличивается при переходе от фторидных к иодидным растворам. [4]
Устойчивость комплексных ионов характеризуется константой устойчивости. [5]
Устойчивость комплексного иона ScHjPCU2 наиболее высокая по сравнению с дигидрофосфатными комплексами других трехвалентных металлов. Так, согласно [5], рренаро 2 2 8 - 10 - 3 при ионной силе ( р), равной 0 46; fWn, po424 49; Рсенаро. [6]
Устойчивость комплексных ионов, которые можно рассматривать как производные хорошо известных комплексных ионов HgXl, уменьшается при переходе от иодидов к хлоридам. [7]
Устойчивость комплексных ионов в расплаве повышается по мере усиления ковалентной природы связи в комплексах, например с увеличением поляризующей способности галогенидных лиган-дов при переходе от хлоридов к бромидам. [8]
Устойчивость комплексных ионов может колебаться в очень широких предела-х. В табл. 71 приведены величины К и pSK некоторых комплексных ионов. [9]
Кроме устойчивости комплексных ионов на порядок вымывания влияет также относительное сродство металла к иониту. Показано, что адсорбируемость ионов редкоземельных элементов на ионите КУ-2 уменьшается от лантана к лютецию. Динамика ионообменного разделения определяется именно этими двумя факторами. Действие их всегда взаимосвязано, поскольку оба они регулируют концентрацию анионов комплексообразующего агента, диссоциирующего в водном растворе. Изменение одного параметра неизбежно влечет за собой изменение другого. [10]
Константы устойчивости комплексных ионов, образующихся из простых ( гидратированных) ионов, например, по реакции М2 2А - МА2, обозначены 02 с нижним индексом, равным числу анионов в комплексе. [11]
Сравнение устойчивости комплексных ионов актиния и таких элементов, как Th, Ra, Pb, Tl, Gs, позволяет найти оптимальные условия их разделения, что составляет основу радиохимического анализа продуктов распада 227Ас и делает возможным определение 227Ас по дочерним элементам. [12]
Чем обусловливается устойчивость комплексных ионов в растворе. [13]
Количественной характеристикой устойчивости комплексных ионов могут служить значения их констант нестойкости, или констант устойчивости, применение которых облегчает рассмотрение способности элементов к комплексообразованию в зависимости от порядкового номера элемента. Например, устойчивость аммиакатов и способность к комплексообразованию от Соа к Си2 повышается, а затем при переходе к Zn2 падает. [14]
Решающее влияние на устойчивость комплексных ионов в растворах оказывает тип химической связи внутри комплексного иона. Поэтому устойчивые комплексные ионы в водных растворах образуют только катионы, характеризующиеся высоким потенциалом ионизации, и анионы, характеризующиеся небольшим электронным сродством. Устойчивость комплексных ионов в водных растворах должна убывать в первом приближении в той же последовательности, что и тенденция к образованию ковалентных связей. Этот ряд примерно совпадает с рядом, найденным Гринбергом [111] для комплексных соединений платины и ртути. [15]
Страницы: 1 2 3 4